Original
Utilidad del pliegue diagonal del lóbulo de la oreja en enfermedad coronaria, un signo simple y eficaz
Usefulness of the diagonal ear lobe crease in coronary disease, a simple and effective sign

DOI:
10.59457/cmf.2022.25.01.org03
CITAR EL ARTÍCULO
Monzó Blasco A, Roca Moya P, Benito Navarro C, Canals Valera C, Seguí Ferrero I, Yuste Aguilar FJ, Molina Aguilar P, Zorio Grima E. Utilidad del pliegue diagonal del lóbulo de la oreja en enfermedad coronaria, un signo simple y eficaz. Cuad Med Forense. 2022; 25(1):33-43. DOI: 10.59457/cmf.2022.25.01.org03Cuad Med Forense. 2022; 25(1):33-43
Enviado: 18.06.22 | Revisado: 07.03.22 | Aceptado: 09.08.22
Resumen
Distintas publicaciones han apuntado el valor predictivo de la presencia del pliegue diagonal del lóbulo de la oreja (PDL) para aterosclerosis coronaria (EAC) severa en ambos sexos, si bien se ha discutido su utilidad en mayores de 60 años. A pesar de la sencillez de su evaluación, no se suele utilizar en la práctica clínica/forense. MÉTODOS: Evaluación sistemática de la presencia de PDL en autopsias forenses. RESULTADOS: 247 casos con 177 hombres (72%), edad media de 64±16 años, muerte violenta en 85 casos (34%), natural en 158 casos (64%) e indeterminada en 4 casos (2%), 17% DM, 33% HTA, 41% con EAC severa, 51% muerte súbita cardiovascular (MSCV) y 26% muerte súbita por cardiopatía isquémica (MSC-I). La presencia de EAC severa se asoció significativamente a hombres, edad≥60 años, HTA, peso cardíaco aumentado y PDL; en el análisis multivariado sólo el PDL y el peso cardíaco aumentado mantuvieron su asociación con EAC severa. El mismo análisis multivariado fue realizado para predecir MSCV y MSC-I. En el primer caso sólo el sexo masculino, peso cardíaco aumentado y PDL y en el segundo caso sólo el sexo masculino, la HTA y el peso cardíaco aumentado mantuvieron la significación estadística. Finalmente, analizamos por separado los grupos de edad<60 años (N=91) y edad≥60 años (N=156), estimando la utilidad del PDL en la detección de EAC severa con Sensibilidad=39 y 56%, Especificidad=88 y 75%, Valor Predictivo Positivo=53 y 70%, Valor Predictivo Negativo=81 y 62%, respectivamente. CONCLUSIONES: La comprobación de la presencia de PDL es fácil, rápida y barata. Su fuerte y consistente asociación independiente con EAC severa y muerte CV debería posicionar este rasgo como un dato importante en la exploración física de los pacientes con sospecha de EAC. En nuestra serie, esta asociación se repitió en el grupo de>60 años aunque con menor peso que en los jóvenes.
Palabras clave: Pliegue diagonal lóbulo oreja; Signo de Frank; Muerte súbita cardíaca; Muerte súbita cardiovascular; Arterioesclerosis; Enfermedad arteriosclerótica coronaria.
Abstract
Different publications have pointed out the predictive value of the presence of the diagonal earlobe crease (DELC) for coronary artery disease (CAD) irrespective of gender, although its usefulness in patients over 60 years has been discussed. Despite the simplicity of its evaluation, it is not commonly used in clinical/forensic practice. METHODS: Systematic evaluation of the presence of DELC in forensic autopsies. RESULTS: 247 cases with 177 men (72%), mean age 64±16.3 years, violent death in 85 cases (34%), natural in 158 cases (64%) and undetermined in 4 cases (2%), 17% DM, 33% hypertension, 41% severe CAD, 51% sudden cardiovascular death (SCD-CV) and 26% sudden death due to ischemic heart disease (SCD-I). The presence of severe CAD was significantly associated with men, age ≥60 years, hypertension, increased heart weight and DELC; in multivariate analyses, only DELC and increased heart weight maintained their association with severe CAD. The same multivariate analyses were performed to predict SCD-CV and SCD-I. In the first case, only the male sex, increased heart weight and DELC, and in the second case only the male sex, hypertension and increased heart weight maintained statistical significance. Finally, we separately analyzed the age groups <60 years (N=91) and ≥60 years (N=156), estimating the utility of the DELC with Sensitivity=39 and 56%, Specificity=88 and 75%, Positive predictive value= 53 and 70%, Negative predictive value=81 and 62% respectively. CONCLUSIONS: Checking for the presence of PDL is easy, fast and cheap. Its strong and consistent independent association with severe CAD and CV death should position this trait as an important finding in the physical examination of patients with suspected CAD. In our series, this association was repeated in the group >60 years, although with less weight than in young people.
Key words: Diagonal earlobe crease; Frank’s sign; Sudden cardiac death; Cardiovascular death; Atherosclerosis; Coronary artery disease.
INTRODUCCIÓN
El pliegue diagonal del lóbulo de la oreja (PDL) es un surco profundo, claramente visible a la inspección ocular, que se extiende desde el trago hasta el pabellón auricular posterior, con un ángulo de 45 grados (1). La clasificación morfológica o gradación del PDL más utilizada se basa en la profundidad y extensión del mismo: grado 1: pliegue ligero; grado 2A: pliegue cutáneo superficial que cubre parcialmente el lóbulo de la oreja al menos hasta la mitad; pliegue 2B: un pliegue cutáneo superficial que cubre completamente el lóbulo de la oreja; 3: un pliegue profundo de la piel que cubre todo el lóbulo (se corresponde con la descripción original de Frank) (2,3,4).
Históricamente, la primera evidencia de este pliegue data del siglo I d.C. cuando NL Petrakis (1980) detectó “escultóricamente” este pliegue en un busto del emperador romano Adriano del Museo Nacional de Atenas (5). Los escritos clásicos sugieren que murió de un fallo cardíaco resultante de su hipertensión arterial (HTA) y enfermedad arteriosclerótica coronaria (EAC) (5).
El mecanismo fisiopatológico subyacente de la producción de este pliegue no está aclarado. Entre los años 70-80, la teoría más aceptada fue la de un aporte deficiente de sangre por falta de irrigación terminal del lóbulo de la oreja. Posteriormente se ha propuesto, como teoría más afianzada, el daño microvascular como posibilidad (4). En los pocos trabajos con histología se ha confirmado una mioelastofibrosis arterial en la base del pliegue y degeneración walleriana en los nervios periféricos, hallazgos que indican un proceso crónico vascular (6,7). Parece que el quid de la cuestión está en el desarrollo embriológico. El lóbulo de la oreja está formado por la fusión del primer y segundo arco faríngeo (los montículos auditivos); todos estos procesos se producen tardíamente en el feto, implicando una vascularización disminuida.
De este modo, el lóbulo de la oreja es una región más susceptible a la hipoxia crónica que otras estructuras superficiales y así, la disfunción endotelial como primer paso de la arterioesclerosis, produciría cambios que podemos en los tegumentos que conducirían al desarrollo del PDL de forma más precoz (6).
La primera descripción en pacientes con EAC se publicó en una carta al editor en el New England Journal of Medicine, escrita por ST Frank en 1973 (8). Por ello, se le atribuye a este autor la primera descripción de la asociación entre el pliegue y la enfermedad cardiovascular (CV), motivo por el cual se le conoce también como el signo de Frank.
Desde entonces se ha seguido investigando y en general comprobando esta asociación en diferentes estudios clínicos (1,9,10,11,12), incluyendo su relación con la patología cerebrovascular (13,14). En estudios autópsicos también se ha estudiado, aunque cabe destacar que son escasos (2,4,12,15,16,17). Por otro lado, y de forma muy minoritaria y en referencias antiguas, otros trabajos niegan dicha relación y lo justifican por la edad o la postura al dormir, mientras que otros sí que aceptan su valor predictivo, pero únicamente restringido a sujetos jóvenes (18,19,2021).
A pesar de la sencillez de su evaluación, no se suele utilizar en la práctica clínica o forense para estimar la posible asociación de EAC. El objetivo de este trabajo ha sido comprobar su utilidad en las muertes súbitas cardíacas (MSC) analizando su asociación al origen isquémico de las mismas.
MATERIAL Y MÉTODOS
Planteamos un estudio de tipo observacional, prospectivo y descriptivo de casos y controles basado en la serie de autopsias realizadas en el Instituto de Medicina Legal y Ciencias Forenses de Valencia durante tres meses (Octubre-Diciembre de 2020). Los criterios de exclusión fueron: menores de 15 años, avanzado estado de putrefacción y/o lesiones traumáticas con afectación craneofacial impeditiva.
Durante estos 3 meses se evaluó sistemáticamente la presencia del PDL. Para minimizar el sesgo interobservador, el equipo prosector responsable de la autopsia (auxiliar de autopsia y médico forense) valoró consensuadamente la presencia del PDL cuando era bilateral y lo suficientemente profundo para equivaler a los grados 2B y 3 previamente establecidos en trabajos anteriores (2–4) (Figura 1). Las variables recogidas fueron: edad, sexo, índice de masa corporal (IMC), antecedentes personales de HTA y diabetes mellitus (DM), la presencia de EAC, de arteriosclerosis aórtica y/o en arterias cerebrales, el peso cardíaco y su relación con el peso corporal y la causa de muerte. Se estimó que el peso cardíaco se encontraba aumentado si superaba el 95% del percentil para el peso corporal (22). La EAC severa se define como la EAC con estenosis mayor al 75% de la luz en al menos una de las arterias coronarias principales (22). La arteriosclerosis aórtica y cerebral se evaluó positivamente si presentaban grados moderado/severo, no incluyéndose la presencia de placas aisladas.
Figura 1. Varios ejemplos de PDL: todos se extienden desde el trago hasta el pabellón auricular posterior con un ángulo más o menos de 45 grados. En este trabajo se ha valorado positivamente la presencia del PDL cuando era bilateral y lo suficientemente marcado, sin detallar la profundidad, irregularidad o multiplicidad del pliegue.
La causa de la muerte se estableció siguiendo criterios clinicopatológicos y forenses, agrupando las muertes súbitas de origen CV (MSCV) con un subgrupo específico de origen isquémico (MSC-I) agudo (definida como EAC con trombosis aguda y/o infarto agudo de miocardio) y otro grupo de MSC-I crónica (definida como EAC con estenosis severa y/o cicatrices de infarto) (22,23).
Las variables discretas se mostraron como porcentajes y se analizaron, según correspondiera, con el test de chi-cuadrado o el test exacto de Fisher. Las variables continuas con distribución normal se mostraron como media±desviación estándar y se compararon mediante la t de Student. Las variables continuas sin distribución normal se mostraron como mediana y rango y se compararon mediante el test U de Mann Whitney. Se incluyó en el análisis multivariado aquellas variables con significación estadística en el univariado y otras consideradas de interés en base a la literatura. Se calculó la sensibilidad y la especificidad del rasgo PDL para sospechar EAC severa en distintos grupos clínicos. Se consideró estadísticamente significativo un valor de p<0,05. Se utilizó el paquete estadístico SPSS versión 23.0 (IBM, Chicago, USA).
RESULTADOS
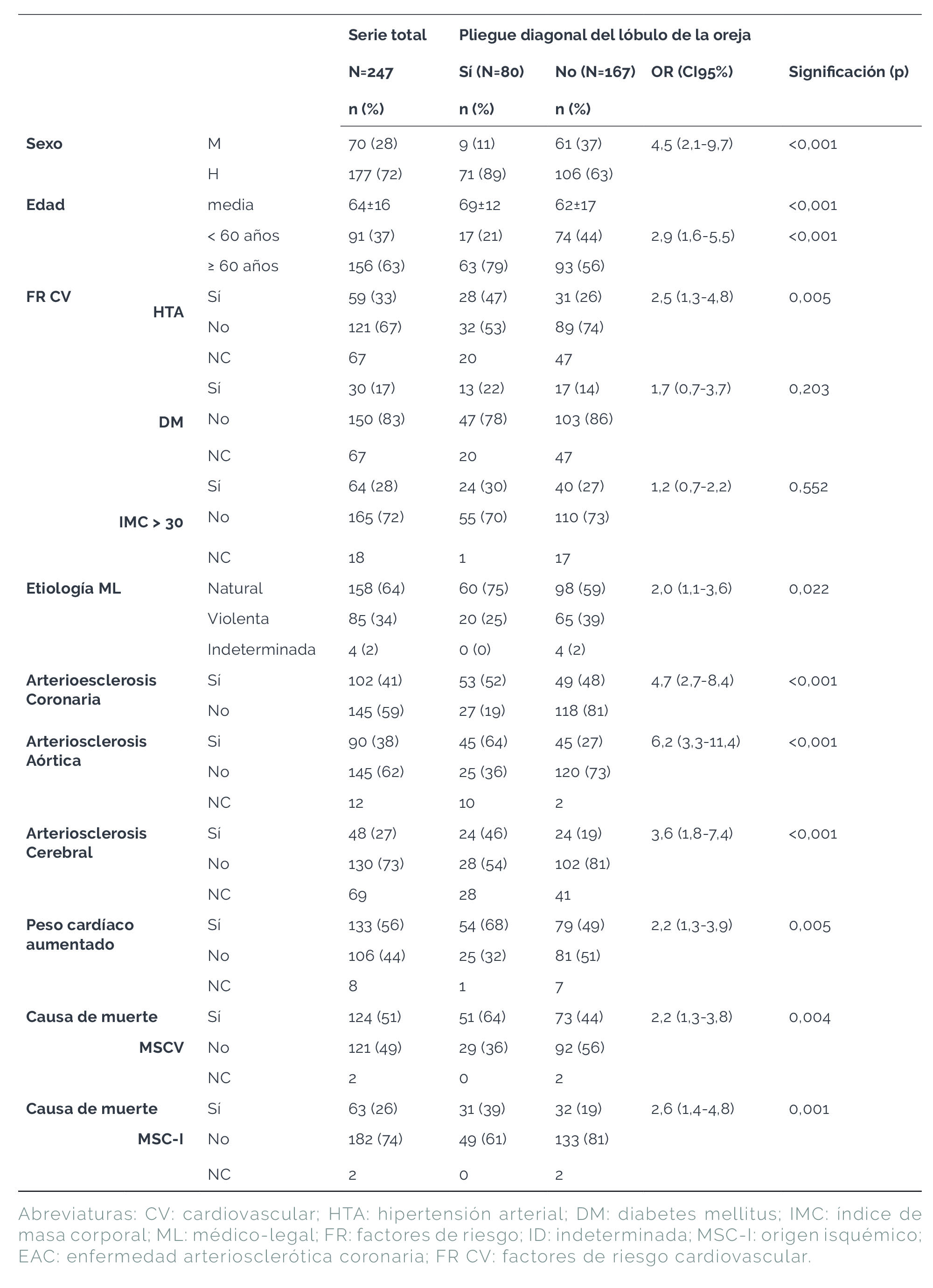
Se estudiaron 247 casos, 177 hombres (72%) con una media de edad de 64±16 años, siendo el 63% de la muestra igual o mayor de 60 años. La etiología medico-legal fue violenta en 85 casos (34%), natural en 158 casos (64%) e indeterminada en 4 casos (2%). Se encontraron antecedentes personales de DM y/o HTA en el 17% y 33% de los casos, respectivamente (datos conocidos en el 73% de la muestra). El PDL se detectó en 80 casos (32%). En la serie completa se comprobó la presencia de EAC severa en 102 casos (41%), arteriosclerosis aórtica en 90 casos (38%) y cerebral en 48 casos (27%) de la muestra. Observamos aumento del peso cardíaco en relación con el peso corporal en 133 casos (56%). Finalmente, del total de casos, 124 (51%) fueron etiquetados de MSCV y, de ellos, 63 (26%) de MSC-I. En la Tabla 1 se muestra la caracterización clínico-forense de la serie.
A modo descriptivo, el análisis univariado mostró que la presencia de PDL se asoció significativamente al sexo masculino, edad avanzada (tanto analizada como variable continua como dicotómica con punto de corte en 60 años), antecedente de HTA, muerte natural, constatación de EAC severa, arteriosclerosis cerebral y aórtica, MSCV y MSC-I pero no se asoció al antecedente de DM o a la presencia de IMC>30 (Tabla 1).
Tabla 1. Caracterización clínico-forense de la serie.
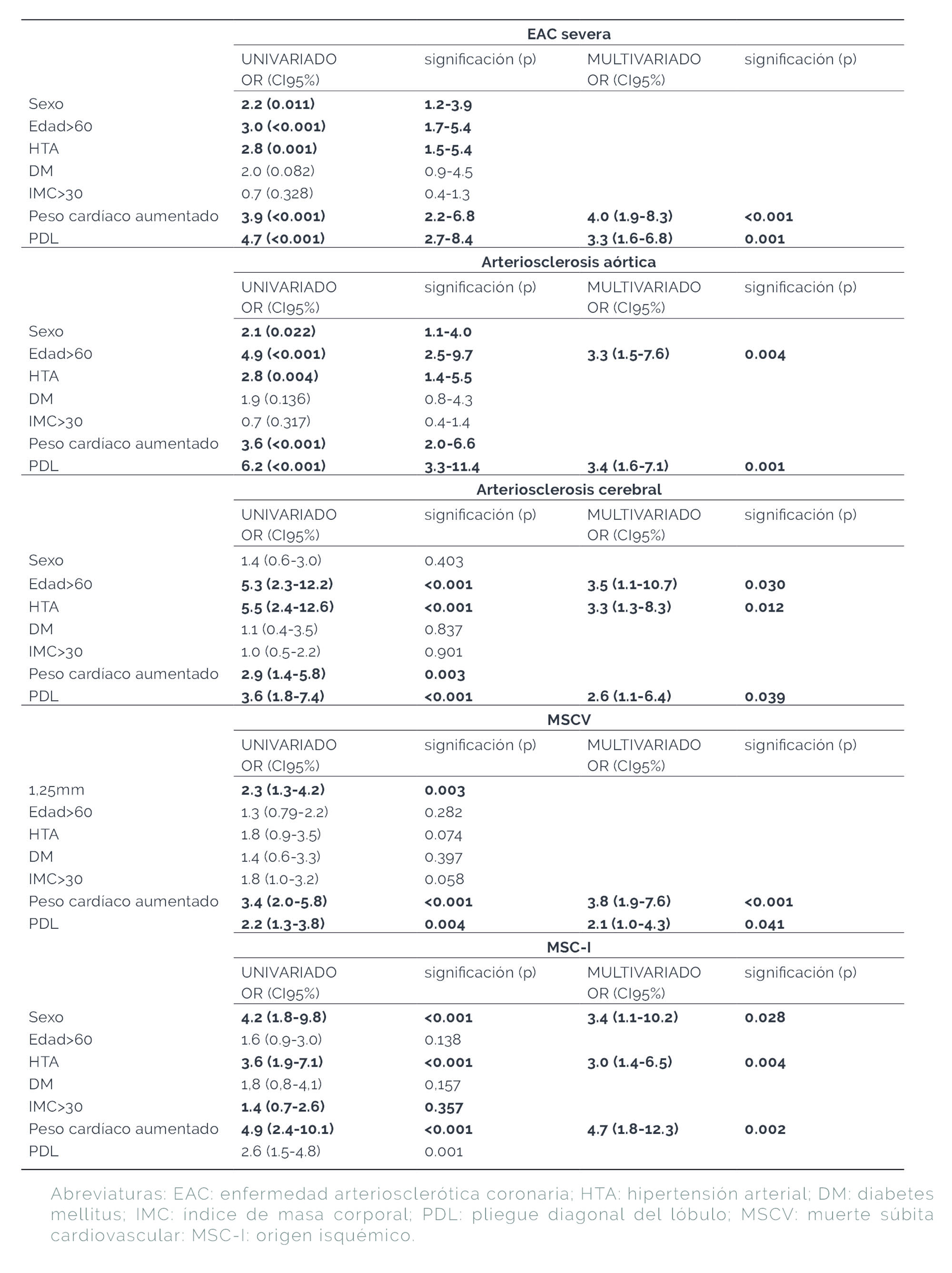
En el análisis univariado los predictores de EAC severa fueron el sexo masculino, la edad ≥60 años, la HTA, la presencia de PDL y el peso cardíaco aumentado, con una tendencia a asociarse a DM (p=0.082) y sin asociación con el IMC>30 (Tabla 2), mientras que en el análisis multivariado incluyendo todos estos factores sólo el PDL (OR=3.3 p=0.001) y el peso cardíaco aumentado (OR=4.0 p<0.001) mantuvieron su asociación con presencia de EAC severa.
Los predictores de la presencia de arterioesclerosis aórtica y cerebral en el análisis univariado fueron similares a EAC severa a excepción del sexo en la arterioesclerosis cerebral. El PDL mantuvo su valor predictivo en el análisis multivariado de ambas localizaciones aórtica (OR=3,4 p=0,001) y cerebral: (OR=2,6 p=0,039) junto con la edad ≥60 años (OR=3,3 p=0,004) en la arterioesclerosis aórtica y junto con la edad ≥60 años (OR=3,5 p=0,030) y la HTA (OR=3,3 p=0,012) en la cerebral (Tabla 2).
Con el mismo análisis multivariado se evaluó la asociación de todas estas variables a MSCV y MSC-I. El PDL (OR=2,1 p<0,041) y el peso cardíaco aumentado (OR=3,8 p<0,001) en el primer caso y el sexo (OR=3,4 p=0,028), la HTA (OR=3 p=0,004) y el peso cardíaco aumentado (OR=4,7 p=0,002) en el segundo caso mantuvieron la significación estadística independiente. El sexo masculino en la MSCV y el PDL en la MSC-I solo se asociaron en el análisis univariado (Tabla 2).
Tabla 2. Resultados del análisis uni/multivariado de las diferentes variables estudiadas en relación con la mortalidad CV, MSC-I y presencia de EAC severa, aterosclerosis aórtica y cerebral.
Como estimación de la utilidad del PDL para sospechar una EAC severa en función de los dos grupos etarios, calculamos una sensibilidad (S) del 39%, una especificidad (E) del 88%, un valor predictivo positivo (VPP) del 53% y un valor predictivo negativo (VPN) del 81% en el grupo de edad <60 años y una S=56%, E=75%, VPP=70%, VPN=62% en el grupo de edad ≥60 años (Tabla 3).
Tabla 3. La sensibilidad, especificidad y los valores predictivos positivos y negativos del PDL para predecir EAC severa por grupos de edad.
DISCUSIÓN
Nuestro trabajo confirma la asociación del PDL con la presencia post mortem de EAC severa tal y como fue previamente descrito en un número limitado de series de autopsias forenses (2, 3,15–17). Algunas de ellas valoran su relación con muertes de origen CV (2,16,17) y, más raramente, se estudia y demuestra su correlación con la presencia de arterioesclerosis aórtica y cerebral (3,4,17) o con el peso cardíaco aumentado (3), resultados todos ellos evidenciados en nuestra serie.
La comparación de los resultados obtenidos en los diferentes trabajos se ve dificultada por las grandes diferencias existentes en estas pocas series publicadas, tanto a nivel muestral como metodológico (Tabla 4). Las autopsias son clínicas o forenses, la valoración en ocasiones se restringe únicamente a la presencia/ausencia del PDL y en otras se analiza su profundidad y bilateralidad y, finalmente, la valoración de la presencia y el grado de EAC es altamente variable.
Tabla 4. Estudio comparativo de las principales series post mortem que estudian la presencia del PDL y su relación con la presencia de arterioesclerosis y/o muerte súbita cardíaca y/o cardiovascular.
En particular, de las cinco principales series post mortem, todas excepto una están realizadas en el ámbito forense, el tamaño muestral varía entre 165-800 casos, la edad media presenta un rango de 34 a 74 años y la frecuencia global del PDL reportada oscila ampliamente de 23 a 72% (2,3,15–17). El método para analizar su presencia incluye tanto la visualización directa en el examen externo de la autopsia como el estudio retrospectivo en fotografías y solo en dos trabajos se utilizan grados para valorar la severidad del pliegue (2,3). El porcentaje de MSC-I es altamente variable en estas series (8-50%) y en todas ellas, excepto en una que únicamente valoran la causa de muerte (16), se demuestra una asociación estadísticamente significativa entre la presencia del PDL y la EAC severa. Es destacable que las series con los porcentajes más altos de PDL coinciden con las que tienen un mayor número de MSC-I (3,16) y edades medias más avanzadas (2,16).
La principal característica de estas series autópsicas es que validan fehacientemente la asociación del PDL con la EAC severa pero no su comportamiento clínico, ya que no se ha demostrado una clara correlación con la MSC-I ni con posibles eventos cardiovasculares anteriores al fallecimiento; aunque esto último podría deberse a la falta de una información clínica completa sobre los casos, que suele ocurrir en patología forense. De este modo, en nuestra serie se observa únicamente el sexo masculino, la HTA y el peso cardíaco aumentado como variables de riesgo de MSC-I con OR de 3,4, 2,7 y 6,6 respectivamente. Aunque el PDL se correlaciona significativamente con el peso cardíaco aumentado (3,6) y con la HTA en nuestra serie, pierde su valor predictivo de MSC-I en el análisis multivariado.
En comparación con las series clínicas más cercanas a nuestro entorno, nuestros resultados muestran una gran similitud con los obtenidos en un estudio hospitalario sobre 1000 pacientes de diferentes servicios médicos. Así, la frecuencia del PDL fue del 33% en pacientes con antecedente de infarto agudo de miocardio o revascularización coronaria frente al 23% que presentaba el grupo sin dicho antecedente (p= 0,001), independientemente de la edad en el modelo multivariado (24). Sin embargo, estos porcentajes fueron significativamente mayores en un estudio de base poblacional con una muestra representativa de la población general adulta, en la que se reportó una frecuencia del PDL bilateral significativamente superior a los dos trabajos previos manteniendo la significación estadística (75,8% vs 54,3%, p< 0,001) (25). Posiblemente, en este último estudio, la mayor frecuencia del PDL en cardiópatas sea debida a la edad media más baja de la muestra (52 ±19 años).
Aunque nuestra serie es pequeña, la asociación encontrada entre el PDL y la presencia de arterioesclerosis, tanto coronaria como aórtica y cerebral, apoya el valor de este signo como marcador de enfermedad aterosclerótica generalizada, no confinada únicamente a las arterias coronarias (14). En esta línea, algunos estudios clínicos más amplios han demostrado con contundencia estadística esta relación más generalizada (13,14,24,26). El hecho de que el PDL sea más común en pacientes con hipertensión arterial y/o diabetes mellitus (16,17) y que se asocie a eventos cardiovasculares independientemente de la edad y el sexo (2,16,17) refuerzan su asociación a aterosclerosis en un sentido global.
CONCLUSIONES
La comprobación de la presencia de PDL es fácil, rápida y barata. Su fuerte y consistente asociación independiente con la presencia de EAC, incluso mayor que para otros factores de riesgo cardiovascular establecidos, debería posicionar este rasgo físico como un dato importante en la exploración física de los pacientes con sospecha de EAC e incidir en un control más estricto sobre aquellos pacientes que lo presenten. Aunque en presencia de una edad avanzada, con mayor probabilidad a priori de EAC, se pierde dicha asociación en algunas series, en el grupo de mayores de 60 años de nuestra serie se mantiene el valor de este signo aunque con menor peso que en sujetos más jóvenes. Este tipo de estudios pone de manifiesto el potencial clínico-preventivo que puede tener la patología forense en el ámbito de la salud pública.
LIMITACIONES
No se han podido incluir algunos factores conocidos de riesgo cardiovascular como el tabaquismo o la dislipemia, por falta de información pre mortem. Algunos datos correspondientes a los antecedentes de HTA y DM así como la presencia de arterioesclerosis aórtica y cerebral no se han podido recoger en todos los casos.
Conflicto de Intereses
Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Fuentes de Financiación
Financiación parcial de Instituto de Salud Carlos III FEDER Unión Europea, Una forma de hacer Europa (PI18/01231, Biobanco La Fe PT17/0015/0043) y Memorial Nacho Barberá
BIBLIOGRAFÍA
- ↑ Agouridis AP, Elisaf MS, Nair DR, Mikhailidis DP. Ear lobe crease: a marker of coronary artery disease? Arch Med Sci. 2015;6:1145-55.
- ↑ V Patel , C Champ, P S Andrews, B E Gostelow, N P Gunasekara, A R Davidson. Diagonal Earlobe Creases and Atheromatous Disease: A Postmortem Study. J R Coll Physicians Lond.1992 Jul;26(3):274-7.
- ↑ Prangenberg J, Doberentz E, Johann L, Madea B. The prognostic value of the Frank sign. Forensic Sci Med Pathol.2022;18:149–155
- ↑ Ishii T, Asuwa N, Masuda S, Ishikawa Y, Shimada K, Takemoto S. Earlobe Crease and Atherosclerosis: An Autopsy Study. J Am Geriatr Soc. agosto de 1990;38(8):871-6.
- ↑ Petrakis NL. Type A Behavior and the Death of Emperor Hadrian. West J Med.1980;132(1):87-91
- ↑ Stoyanov GS, Dzhenkov D, Petkova L, Sapundzhiev N, Georgiev S. The Histological Basis of Frank’s Sign. Head Neck Pathol.2021;15(2):402-7.
- ↑ Shoenfeld Y, Mor R, Weinberger A, Avidor I, Pinkhas J. Diagonal Ear Lobe Crease and Coronary Risk Factors. J Am Geriatr Soc.1980;28(4):184-7.
- ↑ Frank ST. Aural sign of coronary-artery disease. N Engl J Med.1973;289(6):327-8.
- ↑ Wang Y, Mao LH, Jia EZ, Li ZY, Ding XQ, Ge PC, et al. Relationship between diagonal earlobe creases and coronary artery disease as determined via angiography. BMJ Open.2016;6(2):e008558.
- ↑ Evrengül H, Dursunoğlu D, Kaftan A, Zoghi M, Tanrıverdi H, Zungur M, et al. Bilateral Diagonal Earlobe Crease and Coronary Artery Disease: A Significant Association. 2004;209(4):271-5.
- ↑Ramos PM, Gumieiro JH, Miot HA. Association between ear creases and peripheral arterial disease. Clinics. 2010;65(12):1325-7.
- ↑ Wu X li, Yang D you, Zhao Y sheng, Chai W hui, Jin M lei. Diagonal earlobe crease and coronary artery disease in a Chinese population. BMC Cardiovasc Disord. 2014;14(1):43.
- ↑ Nazzal S, Hijazi B, Khalila L, Blum A. Diagonal Earlobe Crease (Frank’s Sign): A Predictor of Cerebral Vascular Events. Am J Med.2017;130(11):1324.e1-1324.e5.
- ↑ Pacei F, Bersano A, Brigo F, Reggiani S, Nardone R. Diagonal earlobe crease (Frank’s sign) and increased risk of cerebrovascular diseases: review of the literature and implications for clinical practice. Neurol Sci.2020;41(2):257-62.
- ↑ Cumberland, Gary D. M.D.; Riddick, LeRoy; Vinson, Richard. Earlobe Creases and Coronary Atherosclerosis The View from Forensic Pathology. Am J Forensic Med Pathol.1987;8(1):9-11.
- ↑ Kirkham N, Murrells T, Melcher DH, Morrison EA. Diagonal earlobe creases and fatal cardiovascular disease: a necropsy study. 1989;61(4):361-4.
- ↑Edston E. The Earlobe Crease, Coronary Artery Disease, and Sudden Cardiac Death: An Autopsy Study of 520 Individuals. Am J Forensic Med Pathol.2006;27(2):129-33.
- ↑ Mallinson TE, Brooke D. Limited Diagnostic Potential of Diagonal Earlobe Crease. Ann Emerg Med.2017;70(4):602-3.
- ↑ Davis TME, Balme M, Jackson D, Stuccio G, Bruce DG. The diagonal ear lobe crease (Frank’s sign) is not associated with coronary artery disease or retinopathy in type 2 diabetes: the Fremantle Diabetes Study. Aust N Z J Med.2000;30(5):573-7.
- ↑ Kenny DJ, Gilligan D. Ear Lobe Crease and Coronary Artery Disease in Patients Undergoing Coronary Arteriography. 1989;76(4):293-8.
- ↑ Gral T, Thornburg M. Earlobe Creases in a Cohort of Elderly Veterans. J Am Geriatr Soc.1983;31(3):134-6.
- ↑ Basso C, Aguilera B, Banner J, Cohle S, d’Amati G, de Gouveia RH, et al. Guidelines for autopsy investigation of sudden cardiac death: 2017 update from the Association for European Cardiovascular Pathology. Virchows Arch.2017;471(6):691-705.
- ↑ Cañadas EV. Gisbert Calabuig. Medicina Legal y Toxicología. 7ª Edición. Elsevier Health Sciences; 2018. 1486 p.
- ↑ Rodríguez-López C, Garlito-Díaz H, Madroñero-Mariscal R, Sánchez-Cervilla PJ, Graciani A, López-Sendón JL, et al. Earlobe Crease Shapes and Cardiovascular Events. Am J Cardiol.2015;116(2):286-93.
- ↑ Ascariz LF. Signo de Frank y riesgo cardiovascular. Un estudio epidemiológico [Internet] [http://purl.org/dc/dcmitype/Text]. Universidade de Santiago de Compostela; 2019 [citado 10 de mayo de 2022]. Disponible en: https://dialnet.unirioja.es/servlet/tesis?codigo=239263
- ↑ Lee JS, Park S, Kim HJ, Kim Y, Jang H, Kim KW, et al. Diagonal Earlobe Crease is a Visible Sign for Cerebral Small Vessel Disease and Amyloid-β. Sci Rep.2017;7(1):13397.
Correspondencia:
Esther Zorio Grima
Servicio de cardiología, Avenida Fernando Abril Martorell , 106 · 46026 Valencia
E-mail: zorio_est@gva.es
Tlf.: 961 245 849