Atlas de Patología Forense
Tromboflebitis en miembro superior como origen de un tromboembolismo pulmonar masivo. A propósito de un caso.
Thromboflebitis in upper extremity as origin of a massive pulmonary embolism. A case report.
Cuad Med Forense. 2005; 11(39):55-61
RESUMEN
El tromboembolismo pulmonar (TEP) masivo es una de las causas de muerte súbita en el adulto que se encuentra con frecuencia nada despreciable en las autopsias forenses. El origen del trombo suele ser una trombosis venosa profunda de las extremidades inferiores en el contexto de una enfermedad tromboembólica venosa. No obstante, en ocasiones, el origen del trombo se encuentra en las extremidades superiores como consecuencia de una tromboflebitis. Presentamos el caso de un paciente ingresado en un hospital, por patología digestiva, en el que se produce una tromboflebitis del miembro superior izquierdo donde portaba una vía intravenosa falleciendo de forma súbita. La autopsia demostró que la causa de la muerte era un TEP masivo. Las implicaciones médico legales del TEP no solo se limitan a determinar la causa de la muerte sino que puede ser necesaria la valoración de una supuesta mala praxis por interposición de una denuncia.
Palabras clave: TEP, Tromboflebitis en miembros superiores, Muerte súbita-inesperada.
ABSTRACT
Pulmonary thromboembolism is commonly associated with sudden death in adults and is a frequent post-mortem finding in forensic autopsies. The emboli aetiology and emplacement are usually related to deep vein thrombosis in lower extremities in the context of a venous thromboembolic disease. However, in some cases, the origin of the thrombus is located in the upper extremities as a result of a thromboflebitis. A case is presented of a patient admitted in hospital with bowel disease who died suddenly after intravenous therapy with thromboflebitis in the left arm. The post-mortem study showed a massive pulmonary embolism as the cause of death. The forensic implications of pulmonary embolism not only imply the investigation of the cause of death but it could also be related, in some cases, to the evaluation of malpractice claims.
Key words: Pulmonary embolism, Venous thrombosis, Sudden-unexpected death.
INTRODUCCIÓN:
El tromboembolismo pulmonar (TEP) consiste en la migración a la circulación pulmonar de un trombo formado en alguna parte del territorio venoso. Debido a la dificultad para efectuar un diagnóstico de certeza, las estadísticas de frecuencia e incidencia existentes son divergentes (aproximadamente se presentan unos 400.000 casos al año en Estados Unidos). Sin embargo, y pese a estas dificultades, está claramente establecido que el TEP constituye una de las principales causa de muerte súbita [1].
Se podría afirmar que este cuadro es uno de los más infradiagnosticados en los casos de muerte en los que no se realiza la autopsia al fallecido. En concreto en Estados Unidos, menos de la mitad de los embolismos pulmonares fatales son reconocidos clínicamente [2].
El origen de la migración embólica puede ser muy diverso, desde las venas hipogástricas, uterinas o desde cavidades cardíacas, sin embargo se puede decir que en un 95% de los casos se trataría de una trombosis venosa profunda de las extremidades inferiores (fundamentalmente localizadas en el hueco poplíteo o en las venas femorales) que, en la mayoría de las ocasiones, se presentarían sin clínica alguna. La morbilidad y la mortalidad de este cuadro es muy elevada, en concreto en Estados Unidos, entre un 0.5 y un 1 % de los pacientes hospitalizados pueden presentar un cuadro de TEP y un 15% de los pacientes que fallecen estando en el Hospital, y se les realiza un estudio postmorten, presentan un cuadro de TEP [3], de los cuales un 70% aproximadamente, no se había sospechado la trombosis venosa profunda de las extremidades inferiores [4].
En muchas ocasiones es fundamental poder detectar el cuadro trombótico periférico para evitar la embolización al territorio pulmonar de forma masiva ya que en la mayoría de las ocasiones, en un 92.5% de los casos según Stein [4] en las que esto ocurre, se produciría la muerte en las dos primeras horas. La realización de un estudio mediante eco-doppler de las venas afectadas puede ser suficiente para descartar un cuadro de trombosis [5, 6].
Presentamos un caso en el que la migración del trombo se produjo desde una localización atípica, una tromboflebitis del miembro superior.
PRESENTACIÓN DEL CASO:
Varón de 77 años que ingresa en un centro hospitalario como consecuencia de un cuadro diagnosticado de enfermedad inflamatoria intestinal. Se inicia tratamiento con esteroides por vía intravenosa pero presenta un pico febril y se cambia la venoclisis de miembro por presentar una flebitis del miembro superior izquierdo. En las 24 horas previas al fallecimiento se le retiró toda la medicación intravenosa, pasando a tratamiento esteroideo oral. Durante el ingreso el paciente se levantaba de la cama y deambulaba con normalidad.
A primera hora de la mañana fue encontrado por el personal de enfermería en situación de muerte con livideces establecidas y con cierta rigidez de miembros superiores. Se envió parte judicial de defunción al considerar que se trataba de una muerte súbita-inesperada cuya causa quedaba pendiente de determinar por la autopsia.
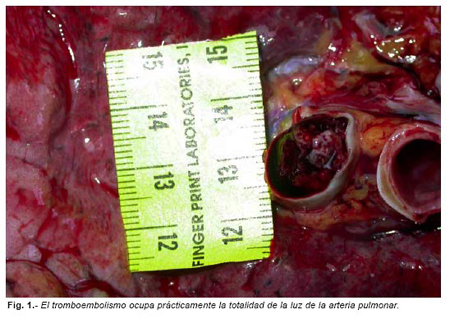
En el examen externo se aprecian venopunciones en ambas flexuras de los miembros superiores con hematoma e induración de la fosa cubital izquierda. En el examen interno se aprecia un trombo de características vitales localizado en ambas arterias pulmonares que se extiende en el pulmón derecho por todas las ramificaciones de la arteria pulmonar hasta las cavidades cardíacas derechas y en el pulmón izquierdo se aprecia claramente como obstruye casi la totalidad de la arteria pulmonar. Al corte del parénquima pulmonar se aprecian restos embólicos en el interior de los vasos de pequeño calibre. Así mismo se observan zonas de edema intersticial y hemorragia pulmonar.
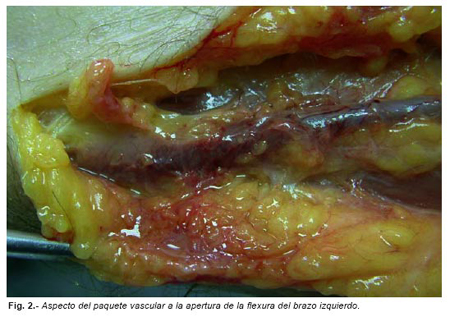
Se procedió a la disección de ambos paquetes vasculares poplíteos, mediante incisión media en el hueco poplíteo, separando los paquetes musculares de ambos gemelos, procediéndose a extraer las arterias y venas poplíteas. En el estudio macroscópico de estas no se apreciaron alteraciones. Por último se procedió a extraer el paquete vascular de la fosa cubital izquierda que presentaba una coloración rojizo-oscura, un engrosamiento y endurecimiento de la vena de dicho paquete y al corte de la misma una formación trombótica en su interior.
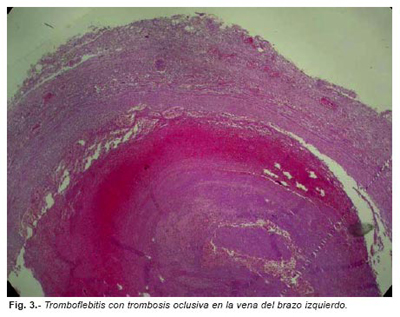
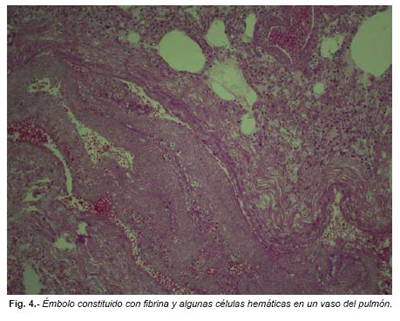
Se realizaron exámenes complementarios en el Departamento de Sevilla del Instituto Nacional de Toxicología y Ciencias Forenses. Los análisis químico-toxicológicos fueron negativos para todas las sustancias estudiadas. En el estudio histopatológico destacaba una congestión vascular generalizada, aterosclerosis coronaria leve con hipertrofia ventricular izquierda y nefroangioesclerosis benigna. En ambos paquetes vasculares poplíteos no se observaron alteraciones histológicas significativas. El paquete vascular del brazo izquierdo mostraba signos de tromboflebitis aguda. En pulmón presentaba congestión y edema, y émbolos de fibrina y algunas células hemáticas en los vasos.
La investigación médio-legal determinó que se trataba de una muerte natural súbita producida por un tromboembolismo pulmonar masivo y que, dado que no existía otro foco, se estableció por exclusión el origen de dicho tromboembolismo en la tromboflebitis del miembro superior izquierdo.
DISCUSIÓN:
El TEP consiste en la migración a la circulación pulmonar de un trombo formado en alguna parte del territorio cardiovascular. El origen de la migración embólica puede ser muy diverso, desde las venas hipogástricas, uterinas o desde las cavidades cardíacas, sin embargo se puede afirmar que en un 95% de los casos se trata de una trombosis venosa profunda de las extremidades inferiores (fundamentalmente del hueco poplíteo y/o de las venas femorales).
Los principales factores de riesgo para la formación de la trombosis venosa profunda y por tanto del TEP se podrían resumir en estos tres [5]:
- Éstasis venosa: Inmovilización como consecuencia de una hospitalización prolongada, de una insuficiencia cardiaca, de una insuficiencia valvular venosa o el cuadro recientemente descrito conocido como el «síndrome de la clase turista». Este se caracteriza por permanecer durante largos periodos de tiempo, por encima de las 4 horas, con las piernas inmóviles en espacios reducidos como ocurre en los aviones durante vuelos prolongados.
- Alteraciones de la íntima venosa (traumatismo directo, enfermedades venosas, cuadros trombóticos previos o cuadros inflamatorios).
- Hipercoagulabilidad por desequilibrio en el sistema de coagulación-fibrinolisis.
Aunque tan solo un 10-20% de los cuadros de trombosis venosas profundas acaban produciendo una lesión pulmonar, el periodo de mayor riesgo sería durante la primera semana (entre 7 y 10 días) decreciendo en el tiempo el riesgo de embolización [1].
Así mismo podríamos decir que existen unos grupos de población especialmente sensibles a la formación de una trombosis venosa profunda y consecuentemente podríamos considerarla como una población de riesgo para sufrir un TEP. Estos grupos serían: ancianos, personas obesas, pacientes que sufren determinadas neoplasias, utilización de anticonceptivos orales, cuadros de deshidratación o antecedentes de enfermedad tromboembólica, siendo de especial gravedad la combinación de varios de estos factores de riesgo.
Las victimas de traumatismos pueden tener mayor riesgo de producción de un TEP que la población general porque [2]:
- Los traumatismos tisulares producen un aumento de la coagulabilidad de la sangre durante varias semanas, sobre todo entre la primera y la segunda semana después del traumatismo.
- La lesión de los tejidos, fundamentalmente a nivel de la pelvis o de los miembros inferiores, pueden originar lesiones musculares o fracturas óseas o lesiones directas sobre las venas que originen una trombosis venosa profunda.
- Los traumatismos suelen confinar a los pacientes en cama durante largos periodos de tiempo o pueden obligarlos a guardar reposo prolongado que originaría un estasis venoso.
Además se ha asociado la mayor frecuencia de presentación de trombosis venosas profundas con el déficit de antitrombina III, proteína C o proteína S así como con la hiperhomocistinemia y el síndrome antifosfolípido. Entre las causas heredadas de hipercoagulabilidad las más frecuentes son las mutaciones en el gen del factor V y el gen que codifica la protrombina. Entre el 2% y el 15% de los individuos de raza blanca se ha detectado una mutación en el gen que codifica el factor V a la que se denomina mutación de Leyden, por ser en esta ciudad de los países bajos donde se descubrió. La consecuencia de esta mutación consiste en la sustitución de una arginina por el residuo normal que es una glutamina en la posición 506 haciendo que la proteína sea resistente a la degradación mediada por la proteína C. Esta resistencia a la inactivación del factor V activado favorece la hipercoagulabilidad. Entre los pacientes con trombosis venosa profunda la frecuencia de portadores alcanza el 60% en algunos estudios.
El cambio de una guanina por una adenina en la posición 21210 del gen que codifica la protrombina se asocia con unos niveles muy elevados de esta y un riesgo de trombosis venosa tres veces superior al de la población general. Esta mutación se detecta en un 1-2% de la población aproximadamente [5, 7, 8, 9].
La migración de parte o en su totalidad de un trombo venoso produce un émbolo que circula a lo largo del drenaje venoso a través de vasos cada vez de mayor calibre hasta alcanzar el corazón derecho, y (a excepción de que el trombo formado sea muy grande y quede retenido en este nivel) suele pasar a través de las válvulas cardíacas del lado derecho y entrar en la circulación pulmonar pudiendo impactar en ambos lados de la bifurcación pulmonar (formando lo que se conoce como «émbolo en silla de montar») o migrar a algunas de las arterias pulmonares más distales. Los émbolos grandes suelen producir cuadros de muerte súbita (siempre que se produzca una obstrucción mayor del 50% de la circulación pulmonar, esto suele ocurrir en un 8-12% de los casos), mientras que los de menor tamaño suelen ocasionar cuadros de hemorragia pulmonar, infartos pulmonares o cuadros de insuficiencia respiratoria leve en aquellos de menor tamaño y de impactación más distal. Así mismo la existencia de una circulación bronquial suficiente puede favorecer la aparición de estos cuadros de infarto pulmonar y de hemorragias pulmonares [10].
Di Maio señala que a la obstrucción mecánica, propia del embolo de la circulación pulmonar, se añade un efecto vasoconstrictor reactivo que reduce aún más la luz de las arterias pulmonares, agravando el cuadro de hipoxia [5].
La consecuencia inmediata es la obstrucción del riego sanguíneo pulmonar hasta las zonas distales del pulmón, lo que originaría por un lado una ineficacia de la oxigenación (aunque el pulmón se encuentre correctamente ventilado, carece de riego sanguíneo para llevar a cabo el intercambio gaseoso) y un aumento del gradiente alveolo-arterial de la PO2, generalmente acompañado de hipoxemia arterial. Todo ello conduce a una hipertensión pulmonar, a una insuficiencia cardiaca aguda (fundamentalmente del ventrículo derecho) y a una disminución del gasto cardíaco que conduciría a la muerte súbita del sujeto si la obstrucción de las arterias pulmonares es masiva. En estos casos los cambios pulmonares macroscópicos que se apreciarían en un estudio postmorten no son significativos [10]. El infarto del tejido pulmonar es raro, ocurriendo solo cuando existe una enfermedad pulmonar subyacente o una cardiopatía [10, 11].
La clínica más frecuente de este cuadro es la disnea de inicio brusco asociado a dolor torácico (fundamentalmente como consecuencia del infarto pulmonar) y a hemoptisis (en casos de hemorragia pulmonar). El síncope brusco asociado a disnea severa puede indicarnos la presencia de un TEP masivo. En un gran número de casos la forma de presentación sería como un cuadro de muerte súbita (a veces no presenciada) [11].
Los émbolos pulmonares suelen ser fácilmente descubiertos durante la realización de una autopsia, procediéndose a abrir la arteria pulmonar, sobre todo cuando se sospeche que la causa de la muerte puede ser ésta, antes de extraer la víscera cardiaca (disección in situ de las arterias pulmonares).
Es importante establecer el diagnóstico diferencial entre un trombo vital y un coágulo postmorten. El émbolo suele ser de consistencia dura o firme, con una superficie estriada e irregular, en la que se pueden diferenciar los depósitos de fibrina, siendo de coloración más grisácea aquellos trombos con mayor data. Aunque suelen tener la forma del vaso que lo aloja adhiriéndose a las paredes de este, a veces presentan forma alargada que pueden indicar la procedencia de una vena periférica. Por su parte el coágulo postmorten, suele ser de color rojo oscuro, gelatinoso y de aspecto brillante en su superficie y se aprecian dos capas claramente diferenciadas, restos de plasma que forman lo que se conoce como «grasa de pollo» y la parte hemática de coloración rojo oscura. Al extraerlo suele retraerse e incluso romperse fácilmente. A veces un émbolo puede tener, a modo de funda, restos de un coágulo postmorten que pueden dificultar el diagnóstico diferencial. Al corte del parénquima pulmonar se puede apreciar en los vasos pulmonares periféricos la presencia de restos de émbolos que ante la mínima presión aparecerían como «pasta de diente saliendo del tubo» [2].
El estudio de las venas periféricas ha de realizarse de forma reglada para considerar la autopsia como completa, debiéndose practicar una incisión en ambos huecos poplíteos, separando la musculatura de la zona y accediendo a ambos paquetes vasculares poplíteos observándose si existen en estos restos trombóticos.
Por otro lado, no debe quedarse el estudio en este punto, si en el examen externo del cadáver se aprecian trastornos tróficos de algunas zonas periféricas o si tenemos antecedentes de vías venosas periféricas, habrá que proceder a su estudio para confirmar si este es o no el origen del embolismo pulmonar. Además, si conocemos los antecedentes de lesiones prostáticas o uterinas o en caso de muertes durante el embarazo o periparto, debemos proceder al estudio de las venas pélvicas, periprostáticas o uterinas para buscar el origen del embolismo pulmonar.
En cualquier caso, aunque el diagnóstico macroscópico sea evidente, la confirmación definitiva de la vitalidad del trombo vendrá determinada por el estudio histopatológico.
Las implicaciones médico-legales del TEP podrían resumirse en los siguientes puntos:
- En aquellos casos de muerte súbita-inesperada.
- En la valoración médico-forense de una denuncia por presunta mala praxis médica.
- En el caso de un TEP secundario y diferido en el tiempo a un traumatismo directo o que como consecuencia de este se produzca una estancia prolongada en cama o un reposo prolongado.
AGRADECIMIENTOS:
A Marisa Vázquez Pereira y Francisco Tovar Alcaide, por sus labores técnicas en el corte y tinción de las muestras.
BIBLIOGRAFÍA:
- Roca Torrent J. y Ruiz Manzano J. Enfermedades vasculares del pulmón. Tromboembolia pulmonar. En Farreras-Rozman. Medicina Interna. Madrid, Ed.Harcourt, 14ª Edición, 2000: 954-968.
- Sauko P y Knight B. Complications of injury. In Bernard Knight´s Forensic Pathology. Third edition. Arnold, London, 2004: 339-351.
- Cook D et al.. Prevention and diagnosis of venous thromboembolism in critically ill patients: a Canadian survey. Crit Care 2001; 5(6): 336-42.
- Stein PD, Henry JW. Prevalence of acute pulmonary embolism among patients in a general hospital and at autopsy. Chest 1995; 108: 978-981.
- Di Maio VJ, Di Maio D. Death due to natural disease. Pulmonary thromboemboli. En Forensic Pathology. Second edition. Boca Raton, Florida, 2001: 94.
- Subramaniam RM, et al. Deep venous thrombosis: withholding anticoagulation therapy after negative complete lower limb findings. Radiology Oct 2005; 237(1): 348-52.
- Thomas R. Hipercoagulability syndromes. Ach Inter Med 2001; 161: 2433-43.
- Poort S et al. A common genetic variation in the 3′-unstranslated region of the prothrombin gene is associated with elevated plasma prothrombin levels and an increase in venous trhombosis. Blood 1996; 88: 3698-3702.
- Vicente V et al. The prothrombin gene variant g20210A in venous and arterial thromboembolism. Haematologica 1999; 84: 356-61.
- Cotran RS, Kumar V y Collins T. En Robbins Patología estructural y funcional. 6ª edición, Editorial McGraw-Hill-Interamericana. Madrid 1999.
- Goldhaber SZ. Tromboembolia pulmonar. En Harrison Principios de Medicina interna. Madrid, Ed. Interamericana-McGraw-Hill, 14ª Edición, 1999:1671.
Correspondencia:
Dr. Sebastián Díaz Ruiz.
Servicio de Patología Forense IML de Málaga.
Parque cementerio, carretera de campanillas s/n. Málaga.
E-mail: sebastian.diaz.ius@juntadeandalucia.es. Tfno: 952 434 720.