Revisión
Patología forense y neurología asociada de los traumatismos craneoencefálicos. Estudio práctico
Forensic pathology and associated neurology of head injury. Practical aspects
Cuad Med Forense. 2008; 14(52):87-118
RESUMEN
Se reúnen en este trabajo de forma sucinta los conocimientos más útiles en la resolución forense de los traumatismos craneoencefálicos (TCE) letales. El estudio está orientado hacia la identificación macroscópica, la causalidad y los mecanismos de producción de las lesiones, con apoyo iconográfico. Se hace especial hincapié en la valoración de las fracturas craneales, las hemorragias subaracnoideas por lesión de la arteria vertebral, el edema y la hiperemia cerebral postraumáticos, así como algunas recomendaciones para la práctica de la autopsia de los fallecidos por trauma cefálico, incluida la retención y fijación del encéfalo. Algunos de estos conocimientos son antiguos y aunque olvidados o desconocidos por muchos han resistido el paso del tiempo, manteniendo plena vigencia. Igualmente se incluyen las características clínicas esenciales de cada trastorno, los nuevos avances en el diagnóstico neuropatológico de los TCE, en su fisiopatología y sus sospechadas relaciones con la posterior aparición de enfermedad degenerativa tipo Alzheimer y las alteraciones genómicas que predisponen a una evolución fatal de TCE ligeros o moderados.
Palabras clave: Traumatismo cráneo-encefálico. Fractura craneal. Hemorragia subaracnoidea. Edema cerebral. Laceración arteria vertebral. Autopsia craneal.
ABSTRACT
This review summarizes in a brief format the most useful tips in the forensic evaluation of fatal head trauma. This study is aimed at the macroscopic evaluation, causality and production mechanisms of the lesions, with image-based support.
Skull fractures, subarachnoid hemorrhage due to lesion of the vertebral artery, posttraumatic cerebral edema and hyperaemia as well as basic recommendations to carry out the autopsy procedure (including the retention and fixation of the brain) in bodies with a lethal traumatic brain injury (TBI) will be analyzed.
Some of this knowledge has been developed a long time ago, and although sometimes forgotten, their meaning is still fully patent.
This study also points out the essential clinical characteristics of each condition and recent advances in the neuropathological diagnosis of traumatic brain injury (TBI) and its physiopathology. Finally, the suspected relationship of head injuries with the late development of degenerative disorders (Alzheimer-like); as well as new insights relating genomics and fatal evolution of mild to moderate TBIs are included.
Key words: Head injury. Skull fracture. Subarachnoid hemorrhage. Cerebral edema. Vertebral artery injury. Craniocerebral autopsy.
1.Introducción
En los países desarrollados los traumatismos constituyen la principal causa de muerte en menores de 40 años, los traumatismos craneoencefálicos (TCE) son responsables de la mitad de estas muertes. Sus causas más frecuentes son: accidentes de tráfico, caídas, agresiones, accidentes de trabajo, domésticos y deportivos.
En EE.UU. cada año se producen unas 52.000 muertes por TCE (18 por 100.000 habitantes). Entre los traumatizados craneales que no fallecen, se producen 100.000 casos que quedan con secuelas permanentes, de ellos 5.000 con epilepsia postraumática y 2.000 en estado vegetativo persistente (EVP) [1 y 2]. En los países industrializados la incidencia es similar.
Los TCE plantean numerosos y complejos problemas médico-legales. Puede ser extraordinariamente difícil ante una herida en el cuero cabelludo o una fractura craneal determinar si se produjo por una caída accidental o una agresión con un objeto contundente; de igual forma, ante una hemorragia subaracnoidea o intraparenquimatosa, establecer si la causa fue una enfermedad o un traumatismo. Con independencia de los antecedentes del sujeto y las circunstancias que condujeron a la muerte, el detenido análisis de las características de las lesiones es imprescindible para la adecuada solución de estos casos. Pese a las dificultades, la cabeza es una de las partes del cuerpo en la que, por las lesiones externas y sobre todo por las internas, mejor se puede deducir el mecanismo de producción de las lesiones.
2.Clasificación
Aunque se han propuesto muchas clasificaciones de los TCE no hay ninguna universalmente aceptada. Para clasificarlos se atiende a una serie de criterios que combinan las causas, mecanismos y consecuencias, tanto estructurales como funcionales. Una división básica es distinguir los traumatismos contusos de los penetrantes, incluidas las heridas por arma de fuego, una causa principal de TCE en algunos países. Similar distinción se realiza entre TCE abiertos y cerrados.
II. 1. Una clasificación útil de los TCE es la que incide en un factor fundamental del mecanismo de producción, como es la existencia o no de impacto sobre la cabeza, es la siguiente [3]:
o LESIONES POR IMPACTO.
Las lesiones resultan del contacto de la cabeza con un objeto.
- Lesiones de partes blandas (erosiones, heridas, etc.)
- Fracturas craneales
- Contusiones cerebrales
- Hematomas epidurales (HED)
- Hemorragias intraparenquimatosas
o LESIONES POR ACELERACIÓN/DESACELERACIÓN. (Sin contacto de la cabeza con un objeto).
La cabeza se ve sometida a un movimiento brusco por una fuerza que ha sido aplicada sobre el tronco o cuello, como cuando el tronco choca con algo y la cabeza se lanza hacia delante.
- Lesión axonal difusa (LAD)
- Hematomas subdurales (HSD)
- Hemorragia subaracnoidea (HSA)
- Contusiones por deslizamiento (Gliding contusions).
Aunque en la mayoría de los casos estas últimas lesiones se producen por un impacto sobre la cabeza, no es imprescindible la existencia del mismo para su producción.
Tipos de aceleración:
El centro de gravedad de la cabeza está situado a nivel de la glándula pineal. Según el desplazamiento de la cabeza en relación con su centro de gravedad el movimiento de aceleración o desaceleración en los traumatismos puede ser lineal, rotatoria o angular.
La aceleración lineal se produce cuando el centro de gravedad se desplaza en línea recta. El ejemplo más típico es el de una persona que viaja en un automóvil a 50 km/h con respaldo alto y la cabeza apoyada sobre el mismo; si el vehículo sufre un alcance posterior por otro que circula a 90 km/h, la cabeza sufrirá una aceleración lineal. En general este tipo de aceleración pura es poco frecuente, porque la unión cráneo-cervical dificulta este movimiento, no suele producir conmoción y, en función de la existencia o no de impacto, puede producir contusiones, hematomas subdurales, etc.
La aceleración rotatoria pura en la práctica es imposible, pues requeriría que la cabeza girara sobre un eje que pasa por su centro de gravedad, ello supondría que todo el cuerpo volteara sobre la cabeza. Puede producirse más fácilmente si la cabeza rota en el plano horizontal, es decir sobre un eje vertical que pase a través de la pineal.
La aceleración angular es la más frecuente y es una combinación de las dos anteriores. El ejemplo más típico es el de un sujeto que estando de pie cae hacia atrás y se golpea contra el suelo. Los traumatismos sufridos por este mecanismo se producen generalmente en los planos frontal y sagital y representan los movimientos más lesivos para el encéfalo. Cuando el movimiento es en el plano frontal, impactos laterales en la cabeza, se produce más daño que si el movimiento es anteroposterior. Por este mecanismo se producen la mayoría de los hematomas subdurales y lesiones axonales difusas.
II. 2. Otras clasificaciones de los TCE se basan en el momento en que se producen las lesiones; si éstas son inmediatas, tras el traumatismo, o aparecen tardíamente.
- LESIONES PRIMARIAS, INMEDIATAS
- Contusiones cerebrales
- Laceraciones cerebrales
- Lesión axonal difusa (LAD)
- LESIONES SECUNDARIAS
- Hemorragias intracraneales
- Hematoma epidural
- Hematoma subdural
- Hemorragia subaracnoidea
- Hemorragia intraparenquimatosa
- Hemorragia intraventricular
- Edema cerebral e Hiperemia cerebral postraumática (Congestive brain swelling)
II. 3. Una última clasificación atiende al carácter focal (contusiones, laceraciones, etc.) o difuso (lesión axonal difusa,) de las lesiones, el edema cerebral puede ser focal o difuso [4].
III. Clínica general de los TCE:
El conocimiento de las manifestaciones clínicas que precedieron a la muerte es necesario para un correcto estudio médico-legal del caso, en ocasiones lo más importante es establecer la correlación clínico-patológica, especialmente las actividades que pudo llevar a cabo el sujeto tras el trauma.
La pérdida de conciencia es habitual en los traumatismos por aceleración/desaceleración de cierta intensidad. Sin embargo, cuando se produce un impacto sobre la cabeza, estando en reposo y no sufre importante aceleración tras el mismo, lo que puede ocurrir en lesiones penetrantes (heridas por proyectiles de baja velocidad) y fracturas hundimiento, sorprendentemente la conciencia puede conservarse inicialmente aun existiendo un gran daño focal (fractura hundimiento y laceración cerebral). En estos casos, sólo hay algunos signos focales como hemianopsia y otros sensitivos de la corteza de los lóbulos parietales y occipitales. Si estas lesiones recaen en lóbulos frontales (o zonas mudas del hemisferio no dominante) el sujeto puede permanecer algún tiempo asintomático, en tanto no se produzca lesión cerebral difusa o daño en el tronco cerebral [5]. Tenemos experiencia de una persona que tras recibir un disparo en la cabeza, por el que murió minutos después, pudo realizar una llamada telefónica relatando lo sucedido después de recibir el disparo.
Los hematomas epidurales, subdurales, edema cerebral e hiperemia cerebral postraumática (congestive brain swelling) pueden cursar clínicamente con intervalos lúcidos. Es decir, que la conservación de la conciencia tras el traumatismo o su recuperación por un tiempo, en las horas o minutos que siguen al trauma, no es infrecuente en casos fatales [6].
La amnesia postraumática anterógrada, también llamada, amnesia postraumática o confusión postraumática, también es un marcador de daño cerebral difuso Es un estado en el que el sujeto muestra un nivel de conciencia aparentemente normal, pero que no disfruta de una memoria continua de los acontecimientos actuales. El sujeto tiene desorientación temporo-espacial y posteriormente no recordará los hechos vividos en esta situación. Esta amnesia puede ser evaluada retrospectivamente en el sujeto vivo mucho tiempo después del accidente. Se le pregunta cuando se dio cuenta por primera vez de donde estaba después del accidente.
La amnesia postraumática retrógrada la experimentan casi todas las víctimas de traumatismos que se acompañan de pérdida de conciencia, desde ligeras conmociones hasta las graves y prolongadas. La amnesia comprende el momento real de la lesión y los hechos inmediatamente anteriores al traumatismo y su duración depende de la gravedad de la lesión.
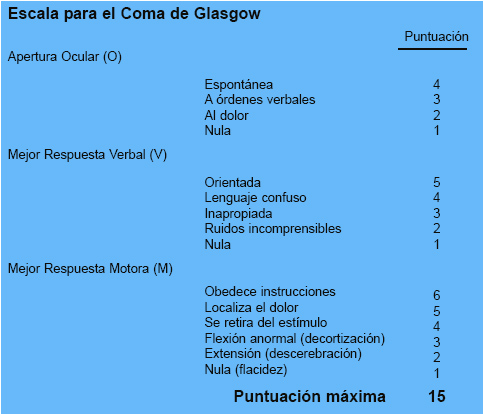
La duración del Coma y la puntuación en la Escala para el Coma de Glasgow son los elementos más utilizados para clasificar clínicamente la gravedad de un TCE. Todo coma de duración superior a 6 horas o puntuación de 8 o menos en la Escala de Glasgow, después de la reanimación, indica la existencia de un TCE grave. La puntuación 13-15 y duración de la inconsciencia menor a 15 minutos es expresiva de TCE leve y de 9-12 e inconsciencia superior a 15 minutos se corresponde con TCE moderado.
La Escala para el Coma de Glasgow es probablemente una de las genialidades de la medicina clínica en las últimas décadas. Desde el año de su publicación, 1974, por Teasdale y Jennet [7], neurocirujanos de la Universidad de Glasgow, a pesar de su uso generalizado en todos los centros médicos del mundo, no sólo no ha sido modificada sino que, habiéndose concebido para el Coma traumático, en la actualidad se emplea también para la valoración del cualquier tipo de coma. El médico forense debe estar familiarizado con la interpretación de sus resultados. La puntuación de 7 o menos indica estado de coma, si la puntuación es de 9 o más no hay estado de coma; el 53 % de los que tienen 8 están en coma.
IV. Lesiones en los TCE:
I. 1. LESIONES DE PARTES BLANDAS
Las lesiones en el cuero cabelludo y en la cara indican los puntos de impacto, pero su ausencia no excluye la existencia de lesiones internas en los TCE.
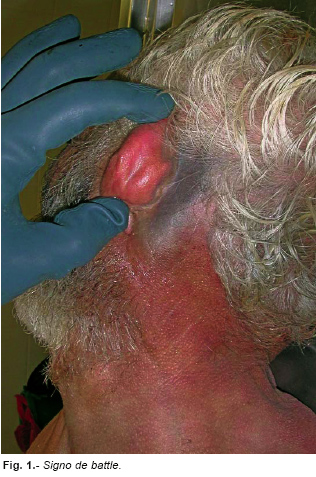
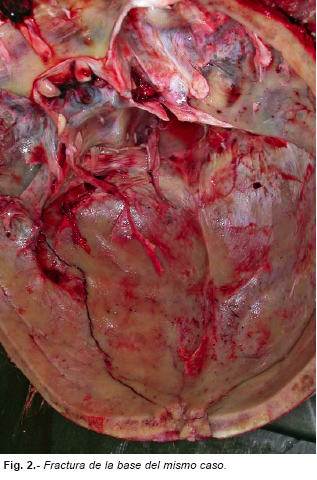
Son de especial significación las equimosis o hematomas palpebrales (ojo morado, hematomas en anteojos, ojos de mapache, etc.) y la equimosis mastoidea (signo de battle), ambos pueden indicar la existencia de una fractura de la base craneal (Figuras nº 1 y 2), pero no siempre; un traumatismo directo o la infiltración de una hemorragia pericraneal desde un nivel superior también pueden ocasionarlos. Para que las hemorragias frontales desciendan a los párpados el sujeto tendría que permanecer en decúbito prono o erguido.
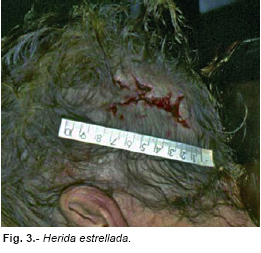
En el cuero cabelludo una caída o un golpe con un objeto contuso pueden dar lugar a una herida con los bordes lisos, como si estuviera producida por un instrumento cortante. Solamente el examen detenido de los bordes y fondo de la herida, mejor con lupa, puede aclarar el origen. Igualmente puede producirse una herida estrellada tanto en una caída o como al ser golpeada la cabeza con un objeto contundente (Figura nº 3), en este caso pueden ayudar las lesiones internas (contusiones cerebrales por golpe o contragolpe), la localización y otros datos.
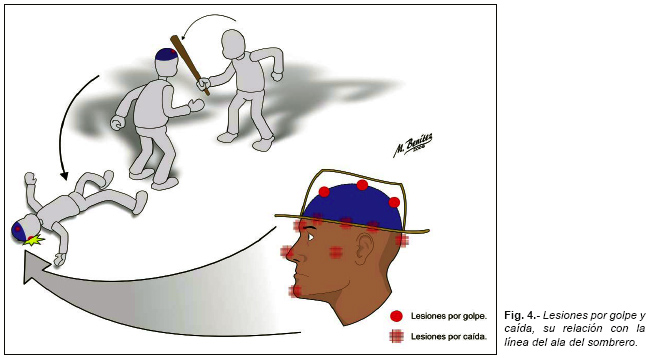
La línea del ala del sombrero [8, 9] es la frontera que separa los traumatismos craneoencefálicos más probablemente producidos por agresión de los más probablemente producidos por caídas (Figura nº 4), aunque con muchas excepciones, ya que en una agresión un sujeto también puede ser golpeado debajo de dicha línea y un sujeto al caer puede, bien en el trayecto o por irregularidad del suelo, lesionarse por encima de dicha línea; lo cierto es que es un dato más de probabilidad que debe tenerse siempre en cuenta. La localización en el lado izquierdo de la cabeza (la mayoría de los sujetos son diestros), salvo agresiones por detrás, y la existencia de múltiples traumatismos, son también más frecuentes en las agresiones.
La línea del ala del sombrero se corresponde con el mayor perímetro horizontal de la cabeza, unos 3 cm. por encima de las cejas y sobre el extremo superior del pabellón auditivo.
Hematomas subcutáneos y subgaleales:
Conviene precisar la localización en el plano en que asientan las hemorragias y hematomas pericraneales; los subperiósticos o cefalohematomas prácticamente solo se ven en el traumatismo obstétrico. En los tejidos blandos pericraneales se pueden ver infiltrados hemorrágicos figurados que reproducen la morfología y tamaño del objeto contundente. Muchas de estas lesiones sólo son visibles cuando se despegan los colgajos del cuero cabelludo. En todo caso cuando se busquen equimosis o erosiones figuradas no debe dudarse en rasurar el cuero cabelludo (Figura nº 5).
IV. 2. FRACTURAS CRANEALES:
Los factores determinantes de la producción de las fracturas craneales son: [3 y 9]
- Características físicas de la cabeza
- Grosor del cuero cabelludo y cantidad de cabello
- Grosor y configuración del cráneo
- Elasticidad del hueso en la zona de impacto
- Características físicas del objeto impactante.
- Forma y tamaño de la superficie de contacto
- Masa del mismo
- Consistencia, estructura de la superficie, rigidez y agudeza de los bordes.
- Cinética del contacto
- Velocidad de la cabeza
- Velocidad del objeto
- Angulo de incidencia
IV.2.1. Principios generales del mecanismo de producción de las fracturas.
La valoración de una fractura craneal encaminada a averiguar su causa y mecanismo de producción debe apoyarse en una serie de principios generales, siendo los más útiles e importantes los siguientes:
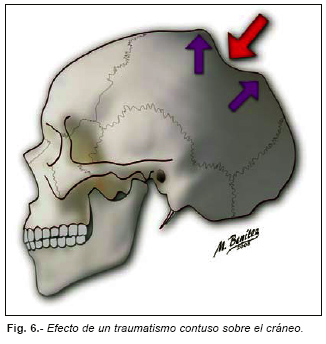
Cuando el cráneo recibe un impacto se comporta como una esfera elástica que se deprime en la zona del impacto y se abomba en las zonas distantes. Si se rebasa el límite de elasticidad se producen las fracturas (Figura nº 6).
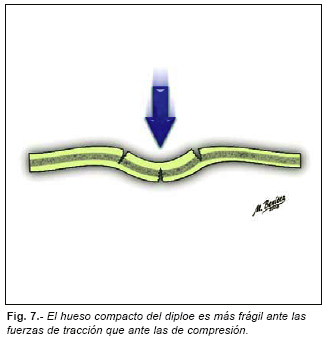
El hueso compacto de las láminas externas e internas del diploe es más frágil ante las fuerzas de tracción que ante las de compresión, lo que explica los puntos de inicio de las fracturas (Figura nº 7).
Un impacto de ligera o moderada energía sobre un área amplia de la bóveda produce más probablemente una fractura lineal. La fractura se inicia a distancia del punto de impacto en la zona que se abomba y si la fuerza se agota no llega a alcanzarlo.
Según la zona del cráneo golpeada un impacto con una misma cantidad de energía determina una fractura lineal o una fractura conminuta.
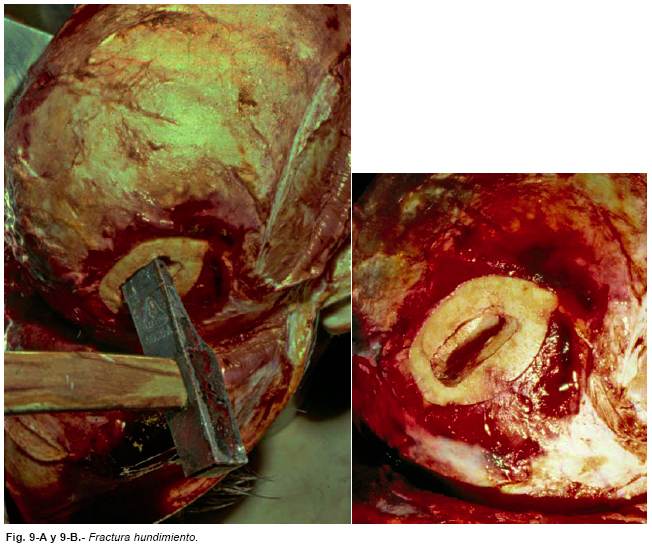
Un impacto de moderada o elevada energía sobre un área pequeña determinará más probablemente una fractura hundimiento (deprimida). La fractura se produce en la zona que se deprime, la del impacto.
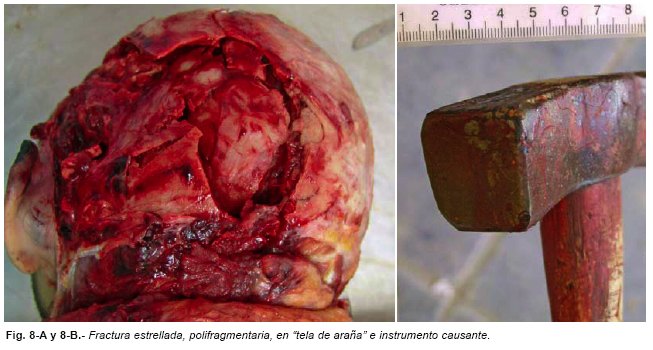
El área de impacto límite que determina que, por un impacto de elevada energía, se produzca una fractura hundimiento o una fractura estrellada, polifragmentaria, son 13 cm2 . Si es mayor, el cráneo en su totalidad se somete a tensión, se deforma y estalla, produciéndose fracturas polifragmentarias (Figura nº 8). Si es menor se produce perforación o hundimiento [9] (Figura nº 9).
Las fracturas estrelladas, polifragmentarias o en «tela de araña», en las que puede haber también hundimiento, se componen de líneas de fractura radiadas que parten del área de impacto y de otras circulares, concéntricas, que lo rodean, lo que es debido al comportamiento de las tablas externas e internas del diploe en las zonas que se abomba y en la que se deprimen [3, 9 y 10].
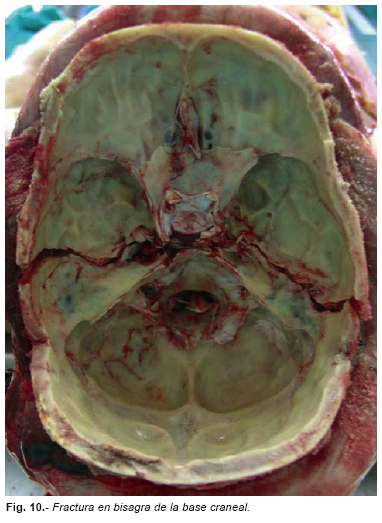
Las fracturas lineales de la bóveda frecuentemente se irradian a la base. Las líneas de fractura discurren siguiendo las zonas débiles y eludiendo las de refuerzo del cráneo (alas del esfenoides, peñascos y el contrafuerte occipital).
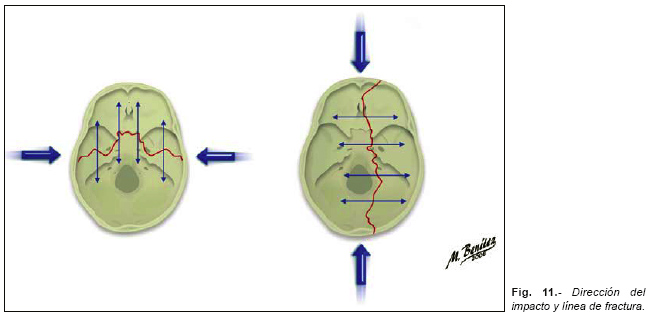
En las fracturas que atraviesan la base del cráneo en sentido longitudinal o transverso (de lado a lado, fracturas en bisagra) (Figura nº 10), la dirección de la línea de fractura suele indicar la dirección del impacto. (Figura nº 11)
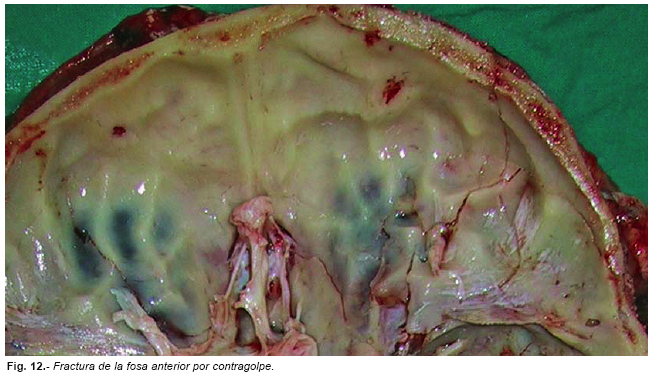
En las caídas hacía atrás pueden producirse fracturas por contragolpe en la fosa craneal anterior, el techo de las órbitas -se trata de las finas láminas óseas que forman el suelo de la fosa craneal anterior- (Figura nº 12). El techo de las orbitas también se fractura en los disparos de arma de fuego en la cabeza, por aumento súbito de la presión intracraneal. Estas fracturas son las típicas causantes de los hematomas palpebrales si el sujeto sobrevive, al menos algunas horas.
Una fractura lineal puede producirse con muy poca energía. En una caída libre, la cabeza cayendo desde 1,80 m. (peso medio de la cabeza humana 4,5 kg), al impactar contra una superficie dura produce energía suficiente para producir una fractura. Un choque de una persona que camina contra un obstáculo en la oscuridad, un golpe con una pelota de golf o una piedra de 100 g sin mucha velocidad pueden ocasionar una fractura craneal.
En los casos de fracturas craneales producidas por más de un impacto sobre la cabeza se puede establecer el orden de producción de los mismos. La regla de Puppe, epónimo del sentido común, dice que si una línea de fractura se detiene en otra, esta se había producido anteriormente. Es decir, la que se detiene es la última en producirse (Figura nº 13)
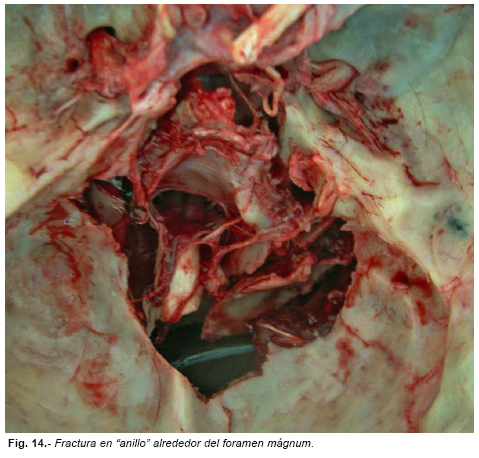
Las fracturas en anillo alrededor del agujero occipital se producen típicamente por impactos sobre la parte superior de la cabeza que empuja el cráneo contra la columna vertebral y también en precipitaciones sobre la extremidad inferior del cuerpo, más raramente por impactos en el mentón (Figura nº 14).
El punto de impacto se deduce de la lesión en las partes blandas tanto del rostro como pericraneales, aunque en muchos casos las hemorragias pericraneales son demasiado extensas para precisar dónde se produjo el impacto que causó la fractura.
Estos son los principios generales que rigen la producción de fracturas y que, junto a las lesiones de partes blandas y encefálicas, permiten en la mayoría de los casos emitir un juicio acertado sobre el más probable mecanismo de producción.
IV.2.2. Características de algunas fracturas:
No hay total correlación entre la producción de una fractura lineal y la gravedad del daño cerebral. Pueden producirse fracturas sin lesión cerebral o pérdida de conciencia, lo que se atribuye a que gran parte de la energía transmitida por el impacto se disipa cuando se fractura el cráneo. Por el contrario, lesiones cerebrales mortales pueden ocurrir sin fractura. El 30% de los fallecidos por TCE no tienen fractura [5]. En todo caso los pacientes con fractura craneal tienen mayor riesgo de sufrir un hematoma intracraneal.
En general, las fracturas occipitales se acompañan con más frecuencia de lesiones intracraneales que las frontales. Se atribuye a que el sujeto en los traumatismos frontales puede protegerse con las extremidades superiores; además los huesos de la cara y los senos paranasales ejercen un efecto absorbente [11].
Fracturas hundimiento o deprimidas.
- El impacto se aplica a una pequeña superficie.
- Se producen en ataques con objetos contundentes o caídas sobre objetos salientes
- Se requiere que el fragmento de la tabla interna se introduzca en la cavidad, al menos el grosor del diploe.
- Se denomina Penetrantesi hay ruptura de la dura y compuestasi hay herida del cuero cabelludo. Las compuestas pueden causar hemorragias masivas que ponen en peligro la vida.
- Se asocian más con epilepsia post-traumática como secuela.
En los niños, por mayor elasticidad del hueso, se producen las fracturas en pelota de ping-pong, realmente un hundimiento del hueso sin que exista solución de continuidad, auténtica fractura.
Fracturas diastáticas:
Las líneas de fractura siguen las suturas de los huesos craneales, esto ocurre sobre todo en sujetos jóvenes.
Fracturas lineales:
- Las más frecuentes.
- Cuando el impacto se aplica sobre una gran superficie.
- Generalmente caídas o accidentes de tráfico.
Fracturas circulares (rodeando el punto de impacto).
Fracturas estrelladas (hundimiento en el punto de impacto).
Fractura en tela de araña. Fracturas conminutas, polifragmentarias.
Fracturas de la base que afectan los senos paranasales o el oído medio; tienen mayor riesgo de meningitis y de fístula de líquido cefalorraquídeo (LCR).
IV. 3. HEMATOMA EPIDURAL (HED)
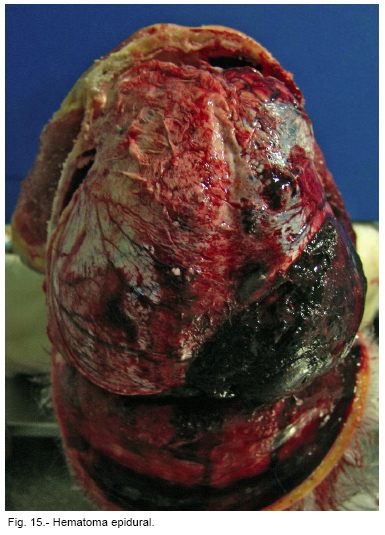
Su incidencia es aproximadamente la mitad que la de los subdurales, siendo cuatro veces más frecuentes en varones que en mujeres. Es una típica lesión por impacto que deforma el cráneo ocasionando despegamiento de la dura del hueso y fractura al menos en el 90 % de los casos. El 10 % restante sin fractura, se trata de niños menores de 15 años en los que, por mayor elasticidad y suturas no totalmente soldadas, se puede producir suficiente deformidad sin fractura. El 85 % de los hematomas se producen por rotura de la arteria meníngea media o sus ramas. La hemorragia arterial diseca la dura de la tabla interna. Los restantes casos son por hemorragia de venas meníngeas media o senos venosos. (Figura nº 15)
Los hematomas epidurales son raros antes de los 2 y después de los 60 años. La incidencia máxima se da entre los 20 y 40 años. La presentación de libro, con intervalo lúcido, solo se da entre el 10 y 27 % de los casos, siendo la duración media de estos de 4 a 8 horas, aunque hay casos de muerte a los 30 minutos. Los hematomas son sintomáticos cuando alcanzan 25 mL y la muerte suele producirse cuando tienen 100 mL, influyendo la velocidad de formación.
Un 20 % de los pacientes con hematoma epidural, también tienen hematoma subdural agudo, lo que agrava el pronóstico.
La mortalidad con óptimo diagnóstico y tratamiento es del 5-10 %, siendo más graves los casos que no tuvieron intervalo lúcido y los que tienen hematoma subdural asociado.
Hematoma epidural por calor:
En las muertes relacionadas con el fuego, el calor intenso produce engrosamiento y contracción de la duramadre y fisuras en ambas tablas de diploe, pudiendo dar lugar a que el contenido hemático de dicho diploe pueda penetrar en el espacio epidural tomando el aspecto de hematoma epidural. El falso hematoma es friable, de aspecto esponjoso por las burbujas y de color marrón achocolatado. Es importante distinguir este artefacto postmortem de un auténtico hematoma epidural por un traumatismo sufrido en vida. La unilateralidad, la existencia de una fractura sobre el hematoma y la ausencia de carboxihemoglobina en el contenido del hematoma son las características generales de un cadáver que murió de un TCE y luego fue quemado.
IV. 4. HEMATOMAS SUBDURALES (HSD):
Las hemorragias en el espacio subdural, entre la dura y la aracnoides, se han clasificado atendiendo al tiempo transcurrido entre el traumatismo y la aparición de las manifestaciones clínicas, los hallazgos en las exploraciones de neuroimagen y el aspecto del contenido del hematoma cuando es drenado. Tienden a organizarse formando pseudomembranas.
- Hematoma subdural agudo
- Dentro de los 3 días siguientes al traumatismo; hematoma compuesto por coágulos de sangre fresca.
- Hematoma sudural subagudo
- Entre el tercer día y la tercera semana; el contenido es una mezcla de sangre fluida y algunos coágulos.
- Hematoma subdural crónico
- Después de la tercera semana; contenido líquido oscuro (como aceite de motor quemado).
Hematoma subdural agudo:
Es una lesión más letal que el hematoma epidural, generalmente por el daño cerebral asociado al hematoma subdural.
Se producen un 72 % por caídas y agresiones y un 24 % por accidentes de tráfico.
La causa más frecuente es la rotura de las venas puente que drenan la sangre de la corteza cerebral a los senos de la duramadre, pero también pueden ser consecuencia de graves contusiones cerebrales y por roturas de arterias de la corteza cerebral.
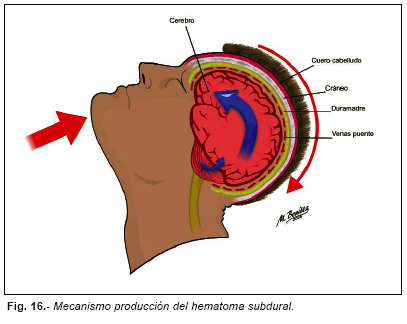
No requieren impacto sobre la cabeza y pueden producirse solo por aceleración o desaceleración de la cabeza (latigazo, zarandeos violentos en caso de tortura, etc.). Si se producen por impacto pueden localizarse en el mismo lado, en el contralateral o ser bilaterales. Al igual que la lesión axonal difusa requiere elevada intensidad de aceleración o desaceleración angular, pero a diferencia de la lesión axonal es más frecuente en los desplazamientos de la cabeza en el sentido antero-posterior y cuando la aceleración o desaceleración se desarrolla en menor tiempo (Figura nº 16).
Predisponen la atrofia cerebral (por ello son más frecuentes en ancianos y alcohólicos), las coagulopatías (incluida la anticoagulación iatrogénica), y en los espontáneos, las malformaciones y tumores (ver HSD espontáneo).
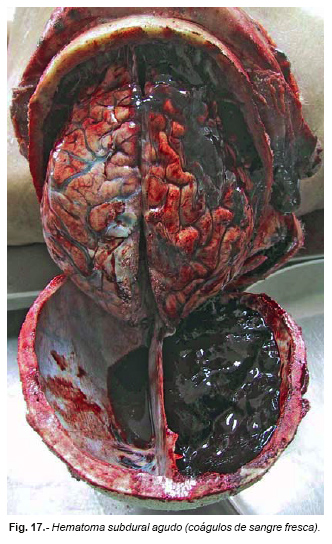
Si se desarrollan rápidamente amenazan la vida cuando alcanzan 50 mL [3], aunque los seguramente mortales tienen más de 120 mL [1] (Figura nº 17).
En las primeras 24 horas el contenido es sangre líquida y coagulada que no se adhiere a la dura. A los 2 – 4 días, los coágulos comienzan a adherirse a la dura.
La sangre de los hematomas epidurales y subdurales puede emplearse para análisis toxicológicos, pues es sangre secuestrada que representa una muestra tomada al tiempo de la lesión. En los hematomas epidurales, sangre arterial, será un reflejo más fiel de la concentración del tóxico en ese momento.
Hay una diferencia entre la superficie encefálica bajo un hematoma epidural o subdural; en el primer caso es lisa y en el segundo se conservan las circunvoluciones.
Hematoma subdural crónico:
En los casos en que un HSD es bien tolerado sin síntomas o serias complicaciones, como la capacidad de reabsorción del espacio subdural es muy limitada, se inicia la organización del hematoma.
A la semana la neomembrana en la cara externa (contigua a la dura) del hematoma es macroscópicamente visible, posteriormente es tan gruesa como la dura.
Los cambios tanto macro como microscópicos en el hematoma son muy precisos y permiten su data.
A partir de las 2-3 semanas el contenido del hematoma se vuelve líquido con color y consistencia de aceite de motor quemado. En el lado subaracnoideo del hematoma se forma una fina membrana sólo de fibrina que con el tiempo es la mitad de gruesa que la del lado dural.
Los hematomas subdurales crónicos pueden ser bien tolerados durante varios meses, pero en cualquier momento pueden experimentar una notable expansión y causar compresión cerebral, lo que se atribuye a hemorragias desde los vasos de la membrana, captación de LCR por ósmosis, etc.
Estos hematomas pueden presentar sintomatología clínica similar a la de los tumores, demencias de instauración rápida, ictus, etc.
Hematoma subdural espontáneo:
Excepcionalmente pueden verse hematomas subdurales en pacientes en los que no es posible identificar un traumatismo previo al que atribuir la lesión. Los síntomas pueden tener un comienzo muy agudo y el paciente puede fallecer. El hematoma puede presentarse de forma aguda, subaguda o crónica. Los factores de riesgo más frecuentes son: hipertensión arterial, anomalías vasculares (malformaciones arteriovenosas, aneurismas), neoplasias, infecciones (meningitis, tuberculosis), alcoholismo, deficiencia de vitamina C, coagulopatías (incluyendo anticoagulación iatrogénica), traumatismos aparentemente inocuos (traspiés, inclinaciones bruscas) o indirectos para la cabeza (latigazo) [11].
Higroma subdural traumático:
Se trata de una colección de líquido cefalorraquídeo en el espacio subdural, casi siempre debida a TCE, más frecuente por caídas o agresiones en sujetos que han consumido alcohol. El líquido puede ser claro, teñido de sangre o xantocrómico. En el 39 % de los casos se asocia a fractura craneal.
El mecanismo de formación generalmente aceptado es un desgarro de la aracnoides que permite la fuga del LCR al espacio subdural; a menudo son bilaterales. También se han descrito casos de higromas como complicación de una meningitis por influenza. Aunque el líquido del higroma puede reabsorberse, si el volumen de la colección continúa aumentando, por un mecanismo valvular, puede producir las mismas consecuencias que un hematoma subdural, es decir efecto masa, con presentación inmediata o semanas después, manifestándose con alteraciones en el estado mental y signos de hipertensión craneal.
Se diferencia del hematoma subdural crónico porque no suele asociarse a contusiones cerebrales, porque el líquido de los higromas contiene pre-albúmina como el LCR, sustancia que no se encuentra en los hematomas subdurales [11], por el contenido sin coágulos oscuros o líquido oscuro (como aceite de motor quemado) propios de los HSD crónicos y sobre todo por la ausencia de membranas en la superficie dural del higroma.
IV. 5. HEMORRAGIAS SUBARACNOIDEAS (HSA)
IV. 5. 1. Hemorragias subaracnoideas traumáticas:
Las hemorragias subaracnoideas (HSA) traumáticas pueden producirse solo por fuerzas de aceleración/desaceleración sin necesidad de impacto sobre la cabeza, aunque la mayoría de las veces se producen por impacto. La hemorragia subaracnoidea traumática generalmente es escasa y se localiza en la convexidad de los hemisferios, sin causar efecto masa. Estas hemorragias se ven en la mayoría de los TCE, incluso en los más leves, y reflejan la rotura de pequeños vasos. Frecuentemente se asocia a contusión cerebral subyacente, pero ambas pueden darse aisladamente, es decir, contusión cerebral sin HSA o HSA sin contusión cerebral. En todo caso la HSA es un indicador de TCE.
La presencia de sangre en el espacio subaracnoideo puede complicarse con hidrocefalia por interferir en la reabsorción del LCR. Las HSA repetidas son causa de hidrocefalia con presión normal que se manifiesta por ataxia, incontinencia de esfínteres y demencia [12].
La acumulación de sangre en el espacio subaracnoideo puede producirse como un artefacto post mortem a consecuencia de la descomposición cadavérica [3]. También, si una vez retirada la bóveda craneal, se retrasa la extracción del encéfalo durante un rato, puede acumularse gran cantidad de sangre en el espacio subaracnoideo de las zonas más declives del encéfalo.
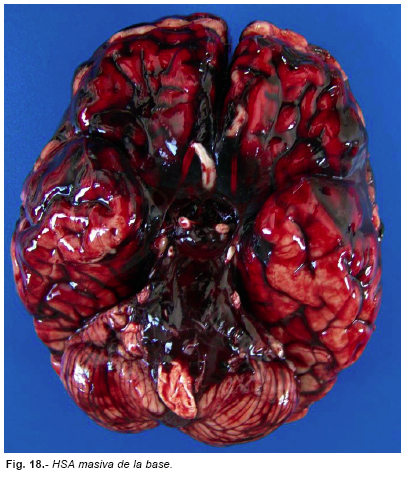
IV. 5. 2. Hemorragias subaracnoideas masivas de la base:
Las hemorragias están localizadas en la cara basal del encéfalo (Figura nº 18). Para que se produzca la muerte fulminante la cantidad de sangre que invade el espacio subaracnoideo tiene que ser del orden de los 100 mL La mayoría de estas hemorragias (75-80 % de las HSA espontáneas) se producen por roturas de aneurismas saculares de las ramas del polígono de Willis y su rotura se relaciona con factores de riesgo: hipertensión arterial, anticonceptivos orales, consumo de cocaína, sexo femenino, hábito de fumar cigarrillos, embarazo, parto, edad, raza negra, etc. [11]. Las HSA de origen aneurismático tienen muy elevada mortalidad (media del 46 %) y la mayoría los pacientes que sobreviven, sin grave o moderada discapacidad, nunca vuelven a tener la misma calidad de vida que antes de la HSA. El síntoma más común de esta HSA es la cefalea («la peor de mi vida», como la describen los pacientes), vómitos, meningismo, incluso síncope.
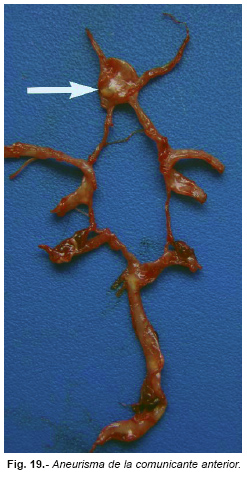
En la mayoría de los casos se suele visualizar el aneurisma roto en la autopsia (Figura nº 19); en los casos que no se localiza se atribuye a rotura de vasos no aneurismáticos o aneurismas pequeños que se destruyen al sangrar. Es preceptivo buscar el aneurisma limpiando toda la sangre con bastoncillos de algodón o un instrumento romo similar, bajo chorro de agua, antes de fijar el encéfalo. Si se fija con la sangre luego será más difícil o imposible localizar el aneurisma.
Otras veces estas hemorragias subaracnoideas masivas aparecen después de un traumatismo y suelen deberse a un desgarro de una arteria vertebral.
IV. 5. 3. Hemorragia subaracnoidea por laceración de la arteria vertebral:
Desde hace muchos años se conoce la posibilidad de que un sujeto pueda sufrir una hemorragia subaracnoidea masiva letal, tras recibir un impacto en la cabeza o en el cuello, por desgarro de una arteria vertebral.
El caso más típico es un varón joven y sano que está bajo los efectos del alcohol y en una pelea recibe un golpe de moderada intensidad en el cuello, se colapsa y muere en pocos minutos. El alcohol actuaría disminuyendo la coordinación neuromuscular, que potencialmente expone la vertebral a excesivo estiramiento, elevando la presión arterial y causando vasodilatación [13]. Se han descrito también muchos casos durante o poco después de un combate de boxeo, en accidentes de tráfico y en los últimos tiempos se han comunicado varios casos ocurridos tras la manipulación de la columna cervical por quiroprácticos [12,13].
El golpe suele recaer en una región lateral o posterior del cuello, menos veces en la cabeza. Los golpes en la mandíbula o laterocervicales altos son los más lesivos. Es muy frecuente encontrar una equimosis en estas regiones, detrás del ángulo de la mandíbula, bajo el pabellón auricular.
El mecanismo del desgarro de la vertebral suele ser la brusca rotación e hiperextensión de la cabeza.
Aunque no es una lesión muy frecuente [14], la laceración de la vertebral puede producirse en el trayecto intracraneal de la arteria (para algunos la mayoría de la veces, aunque no evidenciable por los artefactos que se producen en la autopsia al extraer el encéfalo) [10] o en el espacio comprendido entre el agujero transverso del atlas y su paso a través de la duramadre occipito-atloidea. En los casos de desgarro extracraneal de la vertebral, la sangre extravasada tras el desgarro sigue el trayecto de la arteria y si alcanza la duramadre penetra en el espacio subaracnoideo, pues en ese punto ambas meninges están unidas [15]. La sangre se localiza también en la cara basal del encéfalo, sobre todo en la fosa posterior.
Aunque la hemorragia subaracnoidea se evidencia fácilmente en la autopsia, demostrar su origen en la laceración de la vertebral es extraordinariamente difícil. Ante cualquier hemorragia de este tipo el patólogo está obligado a buscar por los medios disponibles el origen de la hemorragia.
Lo primero para ello es reconocer la posibilidad del desgarro traumático de la vertebral en su trayecto intra o extracraneal, por lo que en un fallecido con los antecedentes referidos en el que se encuentra una hemorragia subaracnoidea masiva al retirar la bóveda, si se dispone de un buen equipo de radiodiagnóstico, lo ideal es hacer una angiografía de la vertebral. Para ello hay que canular las arterias vertebrales en el cuello (las primeras ramas de las subclavias) y si es posible también las vertebrales intracraneales. Como medio de contraste no se pueden utilizar los habitualmente empleados para estudios angiográficos en los sujetos vivos, recomendándose bario en suspensión de gelatina. Si se demuestra el escape del contraste, a continuación se recomienda extraer en bloque la columna cervical y el occipital alrededor del foramen mágnum, fijarlo en formol durante unos días y luego proceder a la disección con lupa binocular.
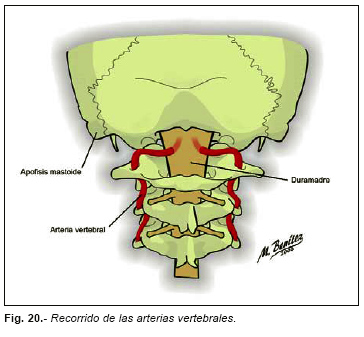
Ante estas dificultades, como los equipos radiológicos no están siempre disponibles, algunos recomiendan ir directamente a buscar el desgarro de la vertebral. Previamente se extrae el encéfalo y se examina para excluir lesiones vasculares intracraneales como causa de la hemorragia subaracnoiea masiva, comprobando la integridad de las vertebrales intracraneales, carótidas internas y sus ramas. El área a visualizar en los casos de lesión extracraneal es la porción de la arteria vertebral comprendida entre el agujero de la apófisis transversa del atlas y su entrada en el espacio subaracnoideo a través de la membrana occipito-atloidea, entre el arco posterior del atlas y el foramen mágnum. (Figura nº 20). El arco posterior del atlas o su apófisis transversa pueden estar fracturados. En los casos de desgarros de la vertebral los músculos profundos de la región pueden estar muy infiltrados de sangre, lo cual también es un signo indicativo de la existencia de la lesión de dicha arteria.
El desgarro debe documentarse con imágenes radiológicas y/o fotográficas y ser confirmado con estudio histopatológico para descartar los artefactos.
Como no hay ningún método generalmente aceptado para la búsqueda de desgarros de la vertebral, la escuela de Sheffield [16] recomienda el método descrito por McCarthy, el cual, tras la retirada de la bóveda, sonda las vertebrales en el cuello e inyecta agua mientras se observa la superficie anterior del tronco cerebral para localizar la fuga de agua.
Para algunos [10], esta lesión de la vertebral extracraneal no ha sido bien conocida hasta hace pocos años, porque esta es una región que normalmente no se diseca en la autopsia y muchas de estas hemorragias subaracnoideas eran atribuidas a roturas de vasos no aneurismáticos o pequeños aneurismas que se destruyen al sangrar y no podían visualizarse en la autopsia.
IV. 6. CONMOCIÓN CEREBRAL (CONCUSSION O COMMOTIO CEREBRI)
Una de las funciones del LCR es proteger al encéfalo de los traumas ligeros, pero cuando la intensidad de los impactos o la aceleración/desaceleración es mayor no puede ser amortiguada y se producen lesiones.
La conmoción es la más leve de todas las alteraciones cerebrales traumáticas, se produce una pérdida de conciencia temporal sin déficit neurológico duradero.
También se define como una alteración de la conciencia debida a un traumatismo craneoencefálico no penetrante; no hay consenso en la duración de los síntomas aunque debe ser breve. No hay alteraciones macro ni microscópicas. La Academia Americana de Neurología considera que la pérdida de conciencia no es necesaria y algunos estudios sugieren que un estado de confusión prolongada, amnesia postraumática, de más de 30 minutos puede indicar más daño que una pérdida de conciencia de unos pocos segundos [11].
Las bases fisiopatológicas del trastorno no son todavía bien conocidas. La lesión inicial produce una serie de alteraciones a nivel celular que desencadenan una cascada de fenómenos neuroquimicos y neurometabólicos. Se produce liberación de radicales libres y neurotransmisores (glutamato, acetilcolina, etc.). Los niveles de glutamato (un neurotransmisor estimulante) se elevan después de la conmoción y un estado hipermetabolico e hiperglucolisis que afecta todo el cerebro después de la conmoción, puede demostrarse todavía 7 a 10 días después de la lesión [11].
En la actualidad se cree que la pérdida de función que acompaña a los TCE se debe a que el trauma induce deformación de la bicapa lipídica de la membrana celular afectando el flujo de iones. El papel de los canales iónicos en estos trastornos se ha subrayado con el descubrimiento de que la mutación de la subunidad CACNA1A se asocia con la producción de coma letal después de lesiones cerebrales ligeras [9].
La sospechada relación directa entre TCE y enfermedad de Alzheimer [17] no pudo ser confirmada en un amplio estudio prospectivo (Estudio de Rotterdam) [18]. La apoliporpoteina E (apoE) se considera responsable del transporte de lípidos dentro del cerebro. Los sujetos que tienen el genotipo e4 de la apoE tienen un riesgo mayor de sufrir trastornos cognitivos con el envejecimiento, además muchos estudios clínicos y experimentales evidencian que la apoE juega un importante papel en la respuesta del cerebro a los traumatismos mecánicos. Se ha propuesto estudiar a los jóvenes atletas para que los que tienen el genotipo e4 de la apoE no practiquen deportes de contacto con alto riesgo de TCE [12].
La conmoción puede ir seguida del Síndrome Post-conmocional, una entidad de mucho interés médico legal.
IV. 7. SÍNDROME DEL SEGUNDO IMPACTO
No es un trastorno frecuente, aunque todos los años se registran uno o dos casos solo en el fútbol americano. Se trata de deportistas que sufren un segundo traumatismo cuando todavía están sintomáticos de uno anterior. Se produce una congestión vascular (Brain Swelling) que progresa a la herniación. Es más frecuente en jóvenes y niños, siendo su mortalidad superior al 50 por 100.
El conocimiento de este trastorno ha dado lugar a la elaboración de protocolos para decidir cuando puede volver a jugar el deportista que ha sufrido una conmoción por leve que sea.
IV. 8. CONTUSIONES Y LACERACIONES CEREBRALES
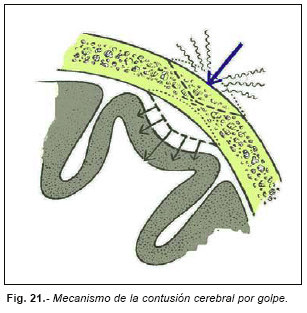
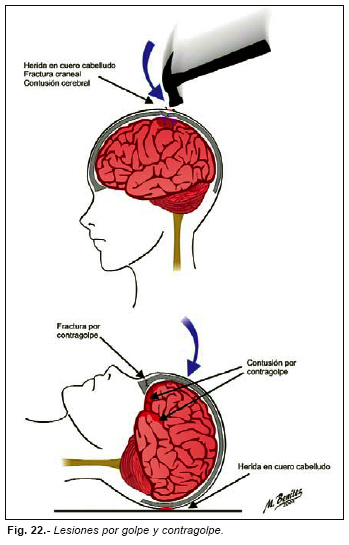
Las contusiones cerebrales son lesiones focales del cerebro por impacto. Generalmente cuando un impacto deforma el cráneo se produce una inflexión de la bóveda que impacta contra la corteza de las circunvoluciones subyacentes. Si se produce fractura, la contusión puede ser más intensa. Este es el mecanismo de las contusiones por golpe. La contusión se encuentra bajo el punto de impacto, típicamente cuando la cabeza es golpeada, estando quieta. (Figura nº 21).
Cuando la cabeza en movimiento impacta contra una superficie dura, se producen contusiones cerebrales en la superficie de los hemisferios diametralmente opuesta al punto de impacto, las llamadas contusiones por contragolpe. Son mas frecuentes en los impactos en los que la cabeza se mueve hacia atrás (caídas), adoptando un patrón tetrapolar, es decir, afectación de los polos de ambos lóbulos frontales y temporales. La explicación más aceptada para estas lesiones es la teoría de la cavitación, según la cual, por desplazamiento del encéfalo, en el sitio opuesto al impacto se produciría una presión negativa que daría lugar a formación de burbujas que al colapsarse ocasionarían el daño tisular, más grave que bajo el punto de impacto. En este puede haber herida y fractura. (Figura nº 22).
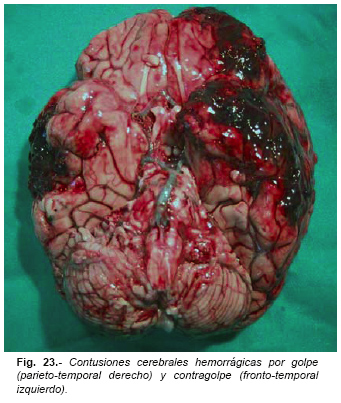
De la misma forma, en las caídas sobre los lados de la cabeza se producen las contusiones por contragolpe en el lado opuesto del cerebro (lóbulo temporal) (Figura nº 23). Este patrón de contusiones por contragolpe es muy útil para distinguir en la autopsia los TCE producidos por golpe de los producidos por caída. Sin embargo, en las caídas hacia adelante no suelen producirse contusiones por contragolpe en las regiones posteriores del encéfalo.
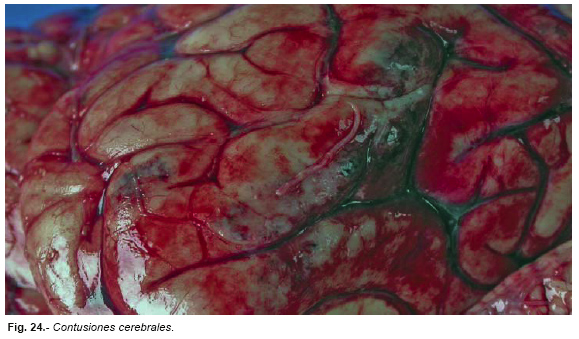
Las alteraciones patológicas de las contusiones son hemorragia (al menos pequeñas hemorragias petequiales en la superficie de la corteza cerebral), edema y necrosis (Figura nº 24). Tienen forma cónica con la base hacia la superficie y el vértice hacia la sustancia blanca. A veces son francas contusiones hemorrágicas.
El término contusión se aplica si la pía está intacta, si se rompe se denomina laceración.
Como lesión focal, las contusiones no tienen por qué acompañarse de pérdida de conciencia y cuando no están asociadas a lesión cerebral difusa tienen escasa morbilidad. Por el contrario muchos TCE fatales se presentan en ausencia de contusiones cerebrales.
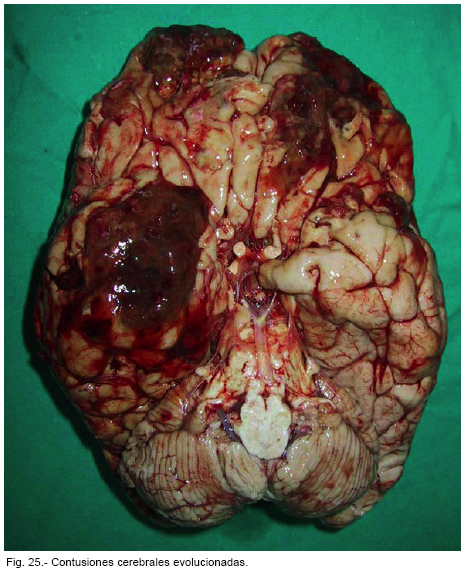
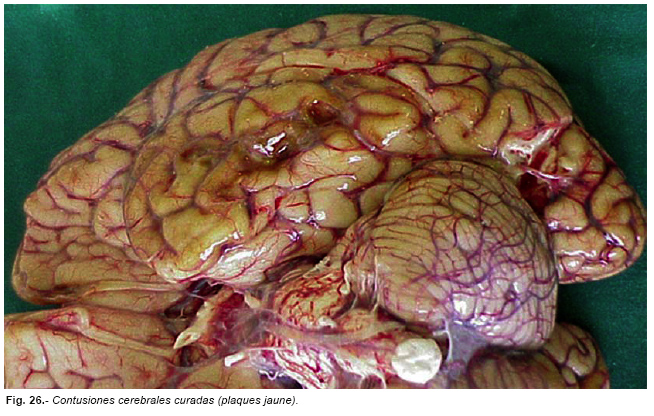
Es posible, dentro de ciertos límites, datar las contusiones cerebrales evolucionadas (Figura nº 25) desde pocas horas hasta muchos años basándose en 18 criterios estructurales, la degeneración neuronal y la reacción leucocitaria, glial y del mesénquima, etc. [19].
Se describen otras contusiones como las intermediarias, por delizamiento (gliding) y la contusión-herniación que no es sino un infarto hemorrágico del tejido herniado.
Las contusiones curadas aparecen macroscópicamente como depresiones pardo-amarillentas teñidas de hemosiderina, placas amarillas (plaques jaune), que persisten durante toda la vida y son hallazgos incidentales en algunas autopsias. (Figura nº 26)
IV. 9 . EDEMA CEREBRAL E HIPEREMIA CEREBRAL POSTRAUMÁTICA (CONGESTIVE BRAIN SWELLING )
La expresión inglesa «Brain Swelling», tumefacción cerebral, se ha aplicado clásicamente al edema cerebral. Desde hace unos años es conocida una complicación de los traumatismos craneoencefálicos consistente en el desarrollo de una tumefacción del encéfalo consecutiva a un traumatismo y debida al incremento del volumen de sangre intravascular cerebral por vasodilatación, sin evidencia de un aumento de agua en el encéfalo como se ve en el edema. A esta complicación algunos la denominan hiperemia o congestión cerebral postraumática o simplemente brain swelling (Congestive Brain Swelling).
El edema y la congestión son trastornos relacionados, ambos pueden ser focales o difusos, afectar sólo la zona lesionada o a uno o los dos hemisferios y tienen las mismas consecuencias, elevación de la presión intracraneal y herniaciones cerebrales que pueden conducir a la muerte o graves secuelas; además la congestión puede evolucionar hacia edema cerebral.
El rápido desarrollo de tumefacción cerebral, pocos minutos u horas después de la lesión, es más probablemente debido a congestión; si la tumefacción se desarrolla dentro de horas o un par de días del trauma es más probable que se trate de edema cerebral [1].
Edema cerebral:
Aunque hay diferentes tipos según la naturaleza del líquido del edema y su localización, los más importantes son el edema vasogénico y el citotóxico. El edema postraumático es el edema vasogénico, la causa habitual es la lesión de la barrera hematoencefálica que permite el paso de líquido al espacio intersticial. El aumento de volumen del encéfalo por edema puede producir un incremento de la presión intracraneal, herniaciones y disminución de la perfusión cerebral hasta la necrosis total del cerebro (muerte cerebral).
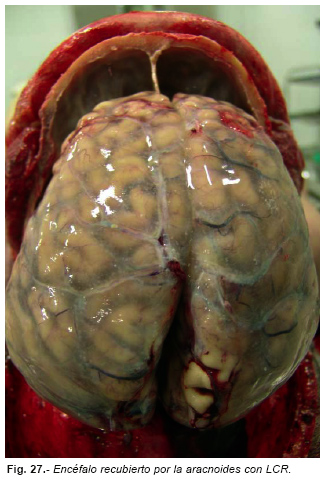
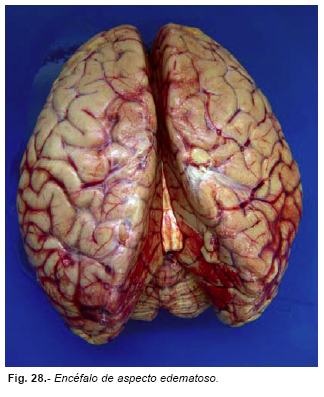
Muchas veces al retirar la duramadre, el cerebro muestra un aspecto como de estar recubierto por una sustancia gelatinosa que desaparece al dar un corte y salir el líquido claro acumulado, lo que no es más que la aracnoides. La cual es mucho más patente en ancianos y alcohólicos, quienes por la atrofia cerebral tienen más amplio el espacio subaracnoideo. Hemos visto a algunos compañeros identificar erróneamente lo descrito como edema cerebral (Figura nº 27). Aunque el diagnóstico de certeza del edema cerebral es esencialmente microscópico, macroscópicamente se caracteriza por circunvoluciones aplanadas y cisuras estrechadas, estando el espacio subaracnoideo colapsado, sin líquido cefalorraquídeo, y apareciendo el cerebro como seco (Figura nº 28); el aumento de peso del encéfalo, la reducción del tamaño de los ventrículos laterales y en su caso los signos de herniación cerebral son signos macroscópicos aun de más valor.
Hiperemia (congestive brain swelling) o congestión cerebral postraumática:
Es un trastorno más frecuente en niños y jóvenes. Puede aparecer inmediatamente después del traumatismo o hacerlo minutos u horas más tarde, con intervalo lúcido. Tiene un comienzo súbito y se cree debido a una pérdida del control de la autorregulación del flujo sanguíneo cerebral (parálisis vascular). Si el acúmulo de sangre en los capilares y vénulas del encéfalo persiste, la elevación de la presión intracraneal puede llegar a niveles letales.
La demostración de este trastorno puede ser difícil en la autopsia pues la caída de la presión arterial que precede a la muerte puede disipar la congestión. Sólo cuando la elevación de la presión intracraneal produce signos de herniación puede probarse. No se debe confundir este trastorno vital con la congestión venosa pasiva postmortem tan frecuente en las autopsias.
En ocasiones la persistencia de la hiperemia puede dar lugar a la rotura de la barrera hematoencefálica y producir edema cerebral vasogénico
IV. 10. HEMORRAGIA INTRAPARENQUIMATOSA:
Hemorragias en la sustancia blanca, contiguas a contusiones cerebrales, pueden verse con cierta frecuencia en los TCE. Son las llamadas contusiones hemorrágicas (contusión-hematoma). El complejo contusión, hematoma y sangre en el espacio subdural se denomina lóbulo reventado («burst lobe»). El 80-90 % de los hematomas intracerebrales traumáticos se producen en la sustancia blanca de los lóbulos frontales y parietales.
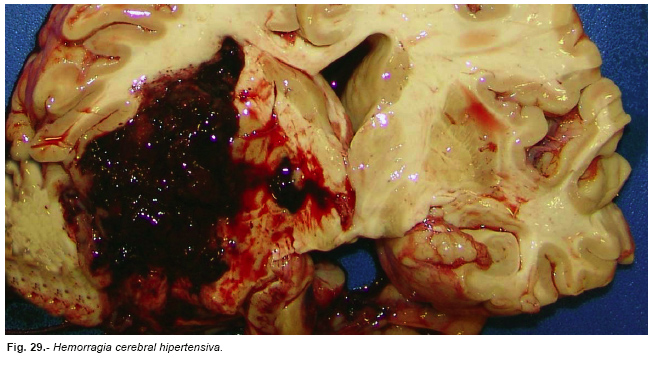
Los hematomas localizados en los ganglios de la base, el diencéfalo, la protuberancia o la sustancia blanca del cerebelo no son traumáticos. Se trata de las hemorragias hipertensivas del adulto (Figura nº 29), debidas generalmente a rotura de los microaneurismas de Charcot existentes en las pequeñas arterias, ramas perforantes en los referidos niveles. La cocaína al elevar la presión arterial puede desencadenar estas hemorragias, como lo puede hacer cualquier otra sustancia que eleve la presión arterial.
La forma denominada HEMORRAGIA CEREBRAL TRAUMÁTICA TARDÍA, se presenta en la mayoría de los casos dentro de las 72 horas desde el traumatismo, aunque se admiten límites de 6 horas hasta 30 días [4]; se atribuyen a coagulopatías, hemorragia dentro de un área de necrosis por reblandecimiento o coalescencia de microhematomas.
En ambos casos los trastornos de la coagulación o la anticoagulación iatrogénica pueden estar implicados.
IV. 11. PRESIÓN INTRACRANEAL (PIC). SÍNDROME DE HERNIACIÓN CEREBRAL:
La hipótesis de Monro-Kellie establece que la suma de los volúmenes intracraneales de sangre, encéfalo, LCR y otros componentes en su caso (hematomas, tumores) es constante y que el incremento de uno tiene que ser compensado con idéntica disminución de otro, si no se eleva la PIC [11]. La elevación de la PIC a ciertos niveles produce desplazamiento del encéfalo, reduce el flujo sanguíneo cerebral y produce un deterioro neurológico.
La mayoría de los pacientes con TCE grave tiene elevación de la presión intracraneal.
Clásicamente se admite que las masas expansivas o incremento de la PIC producen desplazamientos del encéfalo a través de las rígidas aperturas del cráneo (herniaciones en el foramen magnum y tienda del cerebelo) que comprimen otras estructuras del SNC.
Todas las lesiones intracraneales que tienden a aumentar de volumen (hematomas, edema, contusiones, etc.) cuando alcanzan determinada intensidad o hay incremento de la presión intracraneal, producen herniaciones cerebrales. Es el resultado final de las lesiones ocupantes de espacio, por consiguiente, una lesión secundaria a otro trastorno. Se trata del desplazamiento del tejido encefálico, distante de la masa expansiva, a un espacio que normalmente no ocupa a través de un orificio de la duramadre. La herniación implica un grado de irreversibilidad porque el tejido herniado es atrapado en su nueva localización.
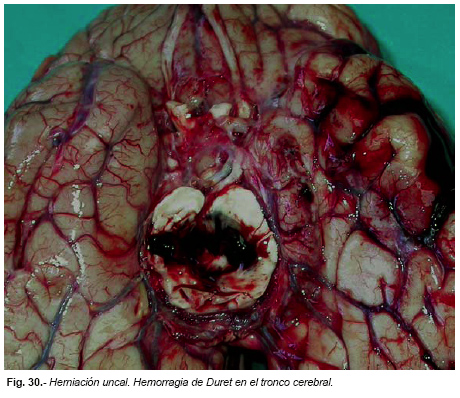
En los síndromes de herniación cerebral se suele comprometer la circulación sanguínea del tejido herniado y del tronco cerebral, dando lugar a lesiones necróticas o hemorrágicas que indican un grado de lesión incompatible con la vida. Los uncus de los temporales y las amígdalas cerebelosas infartadas y hemorrágicas, y las hemorragias de Duret (Figura nº 30) en el tronco cerebral, son el mayor exponente de estos fenómenos en la autopsia.
En todo caso las consecuencias dependen del volumen de la masa expansiva y la velocidad con que se forma.
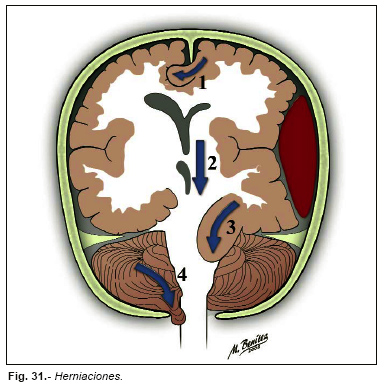
Se distinguen los siguientes tipos de herniaciones según el lugar en el que se producen (Figura nº 31).
- Subfalciforme o supracallosa, bajo la hoz del cerebro.
- Central, transtentorial.
- Uncal, lateral a través de la tienda del cerebelo.
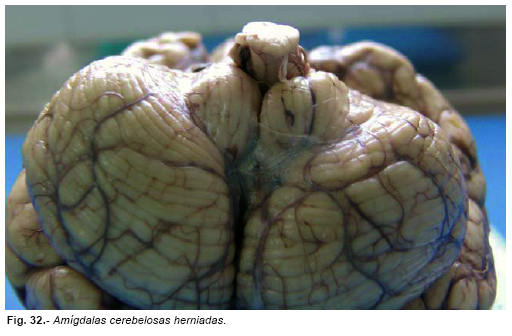
- Amígdalas cerebelosas, por el foramen mágnum (Figura nº 32).
También la craneal o externa (a través de un defecto óseo traumático o quirúrgico).
IV. 12. LESION AXONAL DIFUSA (LAD):
Es la forma más grave de lesión cerebral difusa postraumática. La magnitud, dirección y duración de la aceleración/desaceleración sufrida por la cabeza tienen consecuencias en el tipo de lesión que producen. A mayor duración de la misma más posibilidad de lesión axonal, por ello cuando la cabeza impacta contra objetos relativamente blandos como el salpicadero de un automóvil es más fácil la producción de una LAD, mientras que si el impacto es contra una superficie dura se produce más probablemente un hematoma subdural. Por ello la causa más frecuente de esta lesión son los accidentes de tráfico. La aceleración lateral es más efectiva en producir LAD que el movimiento en el plano sagital, anteroposterior. Las fuerzas de tensión a la que se ven sometidos deforman y dañan los axones, produciéndose desgarros de los mismos en la sustancia blanca subcortical.
Se manifiesta clínicamente por un coma de inicio inmediato tras el trauma y que dura más de 6 horas, nunca hay intervalo lúcido.
A su vez los cuadros de LAD se clasifican por su gravedad en tres grados [20]:
La situación de los que no fallecen en la fase aguda y despiertan del coma puede variar desde secuelas neurológicas leves hasta el Estado Vegetativo Persistente (EVP), denominación propuesta por primera vez por Jennett y Plum en 1972 [21].
La LAD es la causa más frecuente del EVP, también llamado Coma Vigil, Coma Depassé y Síndrome Apálico.
En las personas que sufren LAD y mueren rápidamente pueden no verse lesiones macroscópicas. Cuando se ven se trata de pequeños focos hemorrágicos en el cuerpo calloso y en el cuadrante dorsolateral de la protuberancia, a menudo afectando el pedúnculo cerebeloso superior.
Los criterios de diagnóstico neuropatológico son los cambios producidos en los axones lesionados.
Las bolas de retracción y la proteína precursora del beta-amiloide (PPA) son las alteraciones características de la LAD. Las bolas de retracción en la sustancia blanca subcortical, cerebelo y tronco cerebral son visibles a las 18-24 horas de la lesión por microscopía óptica. Son los extremos de los axones seccionados con un aspecto globular y eosinofílicos. La presencia de la PPA, que se objetiva por técnicas histoquímicas, es el indicador más fiable y precoz del daño axonal, bastando que el sujeto haya tenido una supervivencia superior a 2-3 horas [10, 12 y 22].
La PPA se produce continuamente en las neuronas y circula por los axones. Si estos se lesionan se afecta el transporte de dicha sustancia y se acumula en el cuerpo de las neuronas y en el axón proximal a la lesión, lo que puede ser detectado por técnicas histoquímicas.
Este daño axonal no es exclusivo de los traumatismos y puede verse en otras lesiones cerebrales por isquemia, tumores, etc.
En los que fallecen meses después de la lesión se produce una perdida de sustancia blanca en los hemisferios y agrandamiento de los ventrículos laterales.
V. Autopsia craneoencefálica
En la autopsia craneoencefálica de los fallecidos por TCE deben tenerse presentes las siguientes recomendaciones.
- Tener disponibles todos los estudios de neuroimagen que se le hubieran practicado en vida al fallecido. Es seguro que en la autopsia del futuro los estudios de imagen post-mortem jugarán también un gran papel.
- Rasurar el cuero cabelludo si se sospechan equimosis o erosiones y en todo caso cuando las heridas hayan de ser examinadas con gran detalle.
- No utilizar nunca martillo o cincel para completar el sierre de la bóveda que debe hacerse solamente con la sierra. Una laceración cerebral producida por la sierra puede diferenciarse fácilmente de una lesión vital, no así una fractura producida al aplicar golpes en la autopsia.
- Medir/pesar siempre hematomas subdurales y epidurales. Algunos recomiendan colocar un recipiente bajo la cabeza para que no se pierda parte del contenido, sobre todo el líquido, pero solo si previamente se ha abierto la cava superior para evitar recoger sangre de los senos venosos.
- Despegar el periostio de la bóveda y la duramadre craneal para visualizar bien las fracturas.
- Hacer análisis toxicológico del contenido de hematomas epidurales y subdurales si está indicado; alcohol, cocaína (si tienen varias horas reflejan las concentraciones al momento de la lesión), carboxihemoglobina (en los casos de cadáveres procedentes de incendios).
- Medir las líneas de fractura.
- Medir el grosor del diploe craneal.
- Tomar muestras microbiológicas si hay meningitis.
- Tomar muestras del encéfalo para análisis toxicológicos (lóbulo occipital no afectado) y un mechón de cabello, si está indicado.
- Fijar el encéfalo junto con la duramadre en todo caso que pueda plantear dificultades. Si hay HSA masiva de la base, buscar aneurismas antes de la fijación.
- Tomar muestra de cabello y sangre para tipificación genética en casos de agresiones con objetos contundentes y atropellos con fuga del conductor.
- Fotografiar todas las lesiones y marcar en diagramas las fracturas y las contusiones cerebrales (son muy recomendables los de Armed Forces Institute of Pathology, disponibles en Internet) [23].
El grosor del diploe craneal en varones jóvenes es, según Knight, en frontal y parietal (entre 6 y 10 mm), temporal (4 mm), occipital línea media 15 mm [10].
Fijación del encéfalo VS problemas por la retención de órganos:
El encéfalo debe cortarse tras haber sido fijado de 2 a 3 semanas en formol. Uno de los problemas que se plantean tras el estudio es ¿qué hacer con el encéfalo? cuando el fallecido ya ha sido inhumado, a veces incluso en el extranjero, o incinerado. Este es un problema que habrá que prever y resolver de la mejor forma posible en cada caso. Tenemos experiencia de fallecidos cuya familia, incluso transcurridos varios meses, ha solicitado el órgano para su inhumación. Los escándalos habidos en el Reino Unido en los hospitales Alder Hey de Liverpool y en el Royal Infirmary de Bristol, que salieron a la luz pública en el año 1999, dieron lugar a numerosas investigaciones (policiales, parlamentarias, etc.) y recomendaciones para la retención del cerebro [24]. A numerosos niños autopsiados en dichos hospitales se les habían extraído y almacenado para estudio los órganos sin consentimiento familiar, algunos de dichos órganos habían sido vendidos o cedidos a centros de investigación. Por lo que al tiempo los familiares de algunos niños demandaron al hospital y organizaron un funeral para cada uno de los órganos recuperados. Aunque en la autopsia judicial en nuestro país la extracción de órganos para su estudio no requiere consentimiento de los familiares, pues la autopsia y estudios complementarios se hacen por orden judicial, es evidente que terminados dichos estudios los órganos han de ser reintegrados al cadáver.
Algunos neuropatólogos recomiendan procedimientos ultrarrápidos que permitan fijar o aumentar la consistencia del encéfalo para cortarlo rápidamente. Uno es introducirlo unos minutos en el congelador para que se endurezca (como la mantequilla) evitando la congelación, y otro es sumergirlo en formol e introducirlo en un horno microondas de tipo doméstico, 20 minutos a potencia máxima y otros 20 minutos con potencia baja (cerebros de niños 10 minutos), luego se deja enfriar y se lava con suero salino, posteriormente se puede cortar [2]. Deben tomarse precauciones para eliminar los vapores emitidos por el formol caliente. En todo caso el uso de microondas puede impedir el uso de técnicas histoquímicas e imunohistoquímicas en los bloques de tejidos [25].
La fijación clásica presenta dos problemas, la deformidad al aplastarse el órgano contra el fondo del recipiente y la alteración por los gases de la putrefacción, que dan al encéfalo un aspecto de queso suizo que puede imposibilitar su estudio. Para evitar lo primero se recomienda pasar un hilo entre el tronco basilar y el tronco cerebral que se fija a las asas del cubo de forma que el encéfalo quede entre dos aguas (el volumen del recipiente debe ser de unos 10 litros); últimamente algunos recomiendan añadir un puñado de sal de cocina al formol que, al aumentar su densidad, hace que el encéfalo no se hunda completamente. El formol en estos casos debe estar al menos al 10 % y cambiarse a los 3 días y luego cada semana. En todo caso en que se fije el encéfalo no debe olvidarse fijar también la duramadre encefálica.
Para evitar la formación de gases de putrefacción se puede enfriar el formol y hacer unas incisiones en el cuerpo calloso y en los cuerpos mamilares que permitan la penetración del formol. Esto último es muy recomendable en los casos de edema.
Una vez fijado el encéfalo se deben hacer cortes coronales de los hemisferios separados 1 cm unos de otros, y cortes horizontales del tronco cerebral con una separación de 0,5 cm y también del cerebelo, el primero sagital a través del vermis y los siguientes parasagitales.
Agradecimientos
A Miguel Benítez por la realización de los dibujos para este trabajo.
Bibliografía
- Shkrum Michael J., Ramsay David A. Forensic pathology of trauma : common problems for the pathologist. Humana Press Inc. Totowa, New Jersey, 2007
- Withwell H L, Forensic Neuropatholgy. Hodder Arnold Publishers. London 2005.
- DiMaio VJM. Forensic Pathology. Second edition. CRC Press LLC. Boca Raton. Florida. 2001
- Youmans, JR. (Ed), Neurological surgery, Vol. 4, Fourth edit. W. B. Saunders, Philadelphia,1996.
- Becker DP. Lesiones de la cabeza. En Tratado de Medicina Interna de Cecil. Vol II, 16 ed. Ed Interamericana. México. 1985.
- Reilly PL, Graham DI, Adams JH, Jennett B. Patients with head injury who talk and die. Lancet. 1975 Aug 30;2(7931):375-7.
- Teasdale, G and Jennett, B. Assessment of coma and impaired consciousness. A practical scale. Lancet, 1974, 2, 81-84.
- Kremer C, Racette S, Dionne CA, Sauvageau A., Discrimination of falls and blows in blunt head trauma: sistematic study of the hat brim line rule in relatio to skull fracture. J Forensic Sci. May 2008. 53 (3) 716-9.
- Oehmichen M, Auer R N, König H G. Forensic Neuropathology and Associated Neurology. Springer-Verlag, Berlin 2006.
- Saukko P, Knight B. Knight’s Forensic Pathology, Third edit.. Arnold Publishers. London. 2004
- Greenberg MS, Handbook of Neurosurgery, Fith edit. Thieme, New York, 2001.
- Spitz WU, Spitz DJ, editors. Spitz and Fisher’s medicolegal investigation of death: guidelines for the application of pathology to crime investigation, Fourth edit. Charles C Thomas, Springfield, IL., 2006.
- Koszyca B, Gilbert JD, Blumbergs PC. Traumatic subarachnoid hemorrhage and extracranial vertebral artery injury: a case report and review of the literature. Am J Forensic Med Pathol. 2003 Jun;24(2):114-8
- Opeskin K, Burke MP, Vertebral artery trauma. Am J Forensic Med Path. Sep 1998, 19(3):206-17.
- Contostavlos DL. Isolated basilar traumatic subarachnoid hemorrhage: an observer’s 25 year re-evaluation of the pathogenetic possibilities. Forensic Sci Int. 1995 May 9;73(1):61-74
- Gray JT, Puetz SM, Jackson SL, Green MA Traumatic subarachnoid haemorrhage: a 10-year case study and review. Forensic Sci Int. 1999 Oct 25;105(1):13-23.
- Granacher RP. Traumatic brain injury: methods for clinical and forensic neuropsychiatric assessment. CRC Press LLC. Boca Raton. Florida. 2003
- Mehta KM, Ott A, Kalmijn S, Slooter AJ, van Duijn CM, Hofman A, Breteler MM. Head trauma and risk of dementia and Alzheimer’s disease: The Rotterdam Study. Neurology. 1999 Dec 10;53(9):1959-62
- Oehmichen M, Walter T, Meissner C, Friedrich HJ. Time course of cortical hemorrhages after closed traumatic brain injury: statistical analysis of posttraumatic histomorphological alterations. J Neurotrauma. 2003 Jan;20(1):87-103.
- Palomo Rando JL, Aspectos Medicolegales de los Traumatismos craneoencefálicos. Universidad de Málaga. 1992.
- Jennet B, Plum F. Persistent vegetative state after brain damage: a syndrome in search of name. Lancet. 1972 Apr 1;1(7753):734-7.
- Lafuente JV Daño axonal difuso: Importancia de su diagnóstico en neuropatología forense. Cuad. med. forense, Jul 2005, no.41, p.173-182
- Armed Forces Institute of Pathology. Armes Forces Medical Examiner-Autopsy Diagrams. On line. Disponible en http://www.afip.org/consultation/AFMES/forms/index.html. Consultado: 06/junio/2008.
- Royal College of Pathologists. Guidance for Retention of Brain and spinal Cord Following Post-Mortem Examination And Where Criminal Proceedeings are in Prospect. London, 2002. Disponible en http://www.rcpath.org/resources/pdf/GUIDELINESBRAIN-ARNedited.pdf. Consultado: 12/junio/2008.
- Sheaff M T, Hospter DJ. Postmortem Techique Handbook, 2nd Edition, Springer-Verlag, London, 2005.
Dirección para correspondencia:
Dr. José Luis Palomo Rando.
Servicio de Patología Forense.
IML de Málaga. Ciudad de la Justicia.
C./ Fiscal Luis Portero s/n. 29010 MÁLAGA.
e-mail: jlpalomo45@telefonica.net